➥ Основная статья: Эпилепсия
При эпилепсии электроэнцефалографическое исследование имеет особенно важное диагностическое значение. Наиболее просто вопрос о наличии или отсутствии эпилепсии решается при обнаружении на ЭЭГ несомненно эпилептиформной или эпилептической активности: острые высокоамплитудные волны, спайки, комплексы спайк-волна, острая волна-медленная волна. Нередко в связи с этим возникает вопрос о том, правомерно ли ставить диагноз эпилепсии или расценивать ЭЭГ как патологическую, если у больного в анамнезе не наблюдалось эпилептических приступов. Следует отметить, что при всей академической значимости этого вопроса его практическое значение относительно мало. Дело в том, что электроэнцефалографическому исследованию, как правило, подвергаются люди с какими-либо патологическими симптомами со стороны нервной системы, и в этих случаях результаты анализа ЭЭГ в совокупности с клиническими проявлениями и данными анамнеза позволяют поставить правильный диагноз.
Вторая возможность обнаружения патологических изменений ЭЭГ — профессиональные медицинские обследования. В этих случаях электроэнцефалографическому исследованию подвергают лиц, работающих в условиях, требующих особенной стабильности в поддержании сознания и направленного внимания, что само по себе предъявляет повышенные требования к физиологическому состоянию мозга обследуемого. Можно с уверенностью считать, что обнаружение явной эпилептиформной активности на ЭЭГ является прямым показателем патологического режима работы мозговых систем. Имеются также данные о том, что в периоды, когда на ЭЭГ наблюдаются эпилептиформная активность или даже периоды высокоамплитудных θ- и δ-волн, отмечается снижение уровня внимания, бодрствования и точности слежения.
Статистические исследования также показывают, что у лиц, перенесших тяжелые инфекционные заболевания или травмы мозга и имеющих на ЭЭГ эпилептиформные проявления, впоследствии эпилепсия в виде развернутого заболевания наблюдается во много раз чаще, чем у лиц, перенесших такие заболевания, но без патологических изменений ЭЭГ. Все это заставляет полагать, что более правильно с клинической точки зрения рассматривать эпилептиформные изменения на ЭЭГ даже при отсутствии клинических проявлений как субклинические эпилептические проявления1.
Изменение активности на ЭЭГ

вспышки заостренных α-(1) и β- (2) колебаний; вспышки θ- (3) и полифазных θ- и δ-колебаний (4).
Поскольку проведение электроэнцефалографического исследования во всей полноте, включая повторные регистрации, исследования во время сна или при отмене противосудорожной терапии, в большом числе случаев практически неосуществимо, важное значение при обследовании приобретают феномены, не относящиеся к собственно судорожной активности. В качестве условно эпилептиформных феноменов, расцениваемых обычно как признаки снижения порога судорожной готовности, могут иметь значение следующие графоэлементы на ЭЭГ (рис.).
- Гиперсинхронный, заостренный по форме α-ритм. Эти колебания имеют частоту нормального α-ритма, соответствующее распространение в мозге и амплитуду, превышающую 100-110 мкВ. Волны имеют заостренные вершины, нередко на фоне регулярных веретен появляются компактные группы α-волн, существенно превышающих амплитуду фона. Гиперсинхронный α-ритм может распространяться также на передние отделы или преобладать по амплитуде в определенной области или в одном полушарии. Принадлежность этого ритма к эпилептиформным проявлениям подтверждена с помощью электрокортикографии, которая показывает, что такие колебания при отведении непосредственно от коры носят характер типичных судорожных разрядов типа острых волн2.
- Гиперсинхронный β-ритм. В норме, как указывалось, амплитуда β-ритма обычно не превышает 15 мкВ. Условно эпилептиформной активностью можно считать β-ритм амплитудой более 35 мкВ. Обычно он представлен в виде веретен, часто распространяющихся за пределы нормальной его локализации (лобно-центральной области). Поскольку он имеет относительно высокую частоту (14-40 Гц), увеличение его амплитуды приводит к преобразованию его в группы острых волн. Следует отметить, что гиперсинхронный β-ритм с амплитудой более 40 мкВ следует рассматривать как явно патологический феномен. Патологический β-ритм необходимо дифференцировать от варианта нормальной ЭЭГ, на которой вместо обычного α-ритма регистрируется ритм 14-20 Гц, имеющий все остальные характеристики α-ритма (см. «Нормальная ЭЭГ взрослого бодрствующего человека»).
- Вспышки высокоамплитудных α-, β-, θ- и δ- или полифазных волн с крутыми фронтами, возникающие билатерально-синхронно или локально на фоне относительно нормальной или дезорганизованной активности.
Ввести формальные различия этой активности от других патологических феноменов довольно трудно, и для их характеристики требуется большой опыт. Феномены этого типа отличаются от неэпилептической патологической активности внезапностью возникновения и исчезновения, явной активацией их при гипервентиляции, резким превышением основного фона по амплитуде (обычно в 3-5 раз).
Клинико-электрофизиологическая характеристика эпилептического приступа
В большинстве случаев синдромокинез типичного генерализованного судорожного приступа (ГСП) включает несколько последовательных стадий.
Инициальная (начальная) стадия приступа
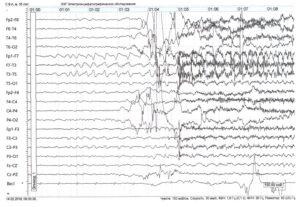
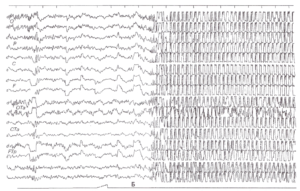
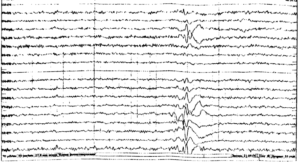
Инициальная (начальная) стадия приступа может сопровождаться вокализацией, отключением сознания (или сумеречным сознанием), падением, судорожными сокращениями мышц грудной клетки. Эта фаза является наиболее важной с точки зрения правильного определения зоны инициации приступа на ЭЭГ, поскольку, как известно, она не всегда соответствует области интериктальных изменений. Одним из характерных графоэлементов начала приступа на ЭЭГ является так называемый «электрический декремент» — депрессия сигнала (снижение амплитуды) в отведениях, соответствующих зоне начала приступа (рис. 1).
Вслед за декрементом должна наблюдаться пространственно-временная эволюция эпилептической активности. Электрографический паттерн должен совпадать с приступом или предшествовать ему с минимальной латентностью.
Тоническая стадия
Далее за начальной стадией у пациента развивается тоническая стадия продолжительностью 15—20 с, сопровождающаяся тоническим напряжением мышц туловища и конечностей. Возможен поворот головы и глаз в сторону, иногда голова запрокидывается, может отмечаться опистотонус, эпизоды апноэ. На ЭЭГ в эту стадию обычно регистрируется разрядная эпилептическая активность. Формально именно активность, регистрируемая во время эпилептического приступа, считается собственно эпилептической активностью (рис. 2).
Клоническия стадия
Далее приступ переходит в клоническую стадию продолжительностью 2—4 мин. У пациента наблюдаются клонические сокращения мышц конечностей, туловища, шумное дыхание. Возможен прикус языка. В большом числе случаев запись настолько искажается миографическими артефактами, что может не подлежать расшифровке (рис. 3). Эта часть эпилептического приступа наиболее опасна с точки зрения риска повреждения оборудования и проводов.
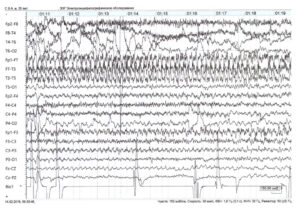
грубая эпилептическая активность
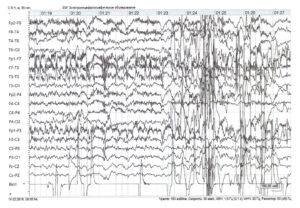
эпилептическая активность, сменяющаяся грубыми миографическими и двигательными артефактами
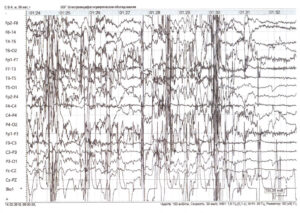
Постприступная стадия
По окончании клонических судорог начинается постприступная стадия. Зрачки, как правило, расширены, отсутствует реакция на свет. Наблюдается мышечная гипотония, отсутствие сухожильных рефлексов. Могут быть непроизвольное мочеиспускание, дефекация. Далее обычно следует сон. На ЭЭГ в этот период может регистрироваться «плоский» паттерн с медленноволновой активностью частотой 0,5—1 Гц крайне низкой амплитуды (рис. 4).
Возможен вариант постприступного периода с развитием психомоторного возбуждения: пациент дезориентирован, отмечается сумеречное нарушение сознания, иногда с агрессией. Больной встает с кровати, пытается куда-то идти, при попытках остановить бурно жестикулирует или отвечает короткими фразами. При этом снижены болевая и температурная чувствительность, что отчасти повышает риск травматизации. Сумеречное состояние может длиться до 30 мин. Вероятность развития психомоторного возбуждения увеличивается, если клоническая стадия была очень короткой или полностью отсутствовала. ЭЭГ в данной ситуации будет мало информативна вследствие большого количества артефактов. Как правило, сумеречное состояние заканчивается сном.
Таким образом, при регистрации ЭЭГ во время эпилептического приступа формируется иктальный паттерн, в той или иной степени искаженный миографическими артефактами. Одним из важнейших характерных признаков для эпилептического приступа является стереотипность регистрируемых эпизодов.
При развитии эпилептического приступа на ЭЭГ регистрируется иктальный паттерн. При длительном (статусном) течении эпилептического приступа регистрируемый паттерн может быть обозначен как ЭЭГ эпилептического статуса. Следует иметь в виду, что иктальный паттерн эпилептического статуса на ЭЭГ не всегда может сопровождаться клинической картиной развернутого судорожного припадка. В таких случаях констатируется формирование бессудорожного эпилептического статуса. Обязательным критерием бессудорожного статуса является отсутствие сознания. Другим вариантом диссоциации электрофизиологической и клинической картины является электрический (эпилептический) статус медленного сна: во время медленного сна регистрируется продолженная генерализованная эпилептиформная активность, не сопровождающаяся моторными эквивалентами.
Дифференциальная диагностика эпилептического приступа и неэпилептических пароксизмальных состояний
Большая длительность обследования при проведении видео-ЭЭГ-мониторинга значительно повышает вероятность регистрации пароксизмального события. Пароксизмальные состояния можно разделить на две основные группы: эпилептического и неэпилептического генеза. Пароксизмальные состояния могут содержать двигательный компонент (который может быть зафиксирован на видеозаписи), а также быть представлены лишь какими-либо субъективными ощущениями пациента (для их регистрации используется кнопка регистрации события у пациента). Неэпилептические эпизоды, сопровождающиеся кратковременным отключением сознания, например в рамках цереброкардиального синдрома, при проведении записи в положении пациента лежа в кровати и отсутствии ЭКГ-регистрации легко могут остаться незамеченными оператором. В дифференциальной диагностике подобных состояний, прежде всего, необходим тщательный сбор анамнеза у пациента (или его родственников) с заполнением анкеты. Необходимо детально описать характер пароксизмов, их частоту, провоцирующие факторы и условия возникновения приступа, продолжительность, способы купирования (если это возможно), характеристику постприступного состояния, наличие или отсутствие сна после приступа, принимаемые лекарственные средства и т. д.
В случае если речь идет о наличии приступов с двигательной активностью у пациента, то, кроме учета данных ЭЭГ, необходимо оценить данные видео- и аудиозаписи.
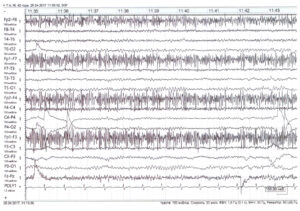
Диссоциация клинических и электрофизиологических данных: клиническое развитие «пароксизмального состояния» не сопровождается регистрацией электрографических признаков иктальной активности
Неэпилептогенные пароксизмы приступов могут успешно маскироваться под генерализованный судорожный приступ, обладая схожими до смешения клиническими проявлениями. Так что зачастую при отсутствии данных ЭЭГ даже опытный эпилептолог будет испытывать большие затруднения в дифференциальной диагностике. Основным решающим фактором в данной ситуации может явиться диссоциация клинических и электрофизиологических данных: клиническое развитие пароксизмального состояния без регистрации электрографических признаков эпилептической активности в ходе выполнения видео-ЭЭГ-мониторинга (рис. 5). Кроме того, наблюдающийся «приступ» иногда быстро купируется введением плацебо (например, физиологического раствора).
Неэпилептические судорожные приступы встречаются чаще всего у женщин (около 70 % случаев), особенно с выраженной психоэмоциональной лабильностью. В подавляющем большинстве припадки происходят при свидетелях (требуют присутствия «зрителей»). Иногда бывает достаточно того, что пациенту известно, что палата оснащена видеокамерой и он находится «под присмотром». Натолкнуть на предположение о неэпилептическом происхождении приступов могут в том числе личностные особенности обследуемого, включая частую смену лечащих врачей «ввиду неэффективности лечения», регулярные вызовы скорой помощи, наличие установленных провоцирующих факторов: психоэмоциональные нагрузки, стрессы и сопутствующие пограничные расстройства личности (например, депрессия, астенизация, тревожные состояния). Для неэпилептических приступов характерна полиморфность описываемых эпизодов: множество разнообразных типов приступов. Пациент указывает на многократные ЭЭГ-исследования с относительно нормальными вариантами биоэлектрической активности или с неспецифическими невыраженными изменениями. Также может настораживать то, что высокая частота тяжелых приступов не соответствует тяжести состояния больного, т. е. отсутствуют неврологическая симптоматика и снижение интеллекта. Отсутствуют травмы, несмотря на указание о перенесенных многократных регулярных тяжелых припадках. У пациента может наблюдаться неэффективность противоэпилептических препаратов или парадоксальное увеличение частоты приступов в ответ на терапию. В то же время может наблюдаться резкий положительный эффект от назначения антидепрессантов и нейропротективных препаратов, а также различных гомеопатических средств. Иногда у пациента может быть образец в виде страдающего эпилепсией родственника или близкого человека.
Функциональные пробы для провокации эпилептической активности
В случае отсутствия в фоновой ЭЭГ эпилептиформных проявлений используют различные способы провокации эпилептической активности с помощью функциональных нагрузок, главными из которых являются ритмическая фотостимуляция и гипервентиляция.
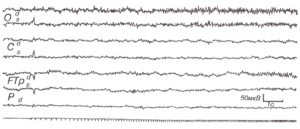
Нижний канал — отметка вспышек света. Наиболее выраженное усвоение — в затылочных отведениях (О), несколько менее выраженное — в задневисочных (Тр) и теменных (Р). Оптимум усвоения — в полосе собственных частот основного ритма ЭЭГ (10- 14/с). В ответ на первую вспышку виден артефакт от вздрагивания.
Фотостимуляция
➥ Более подробно читайте статью: Ритмическая фотостимуляция
Световая ритмическая стимуляция на разных частотах вызывает появление на ЭЭГ ритмических ответов разной степени выраженности, повторяющих ритм световых мельканий. В результате нейродинамических процессов на уровне синапсов, кроме однозначного повторения ритма мельканий, на ЭЭГ могут наблюдаться явления преобразования частоты стимуляции обычно в четное число раз. Важно, что в любом случае возникает эффект синхронизации активности мозга с внешним датчиком ритма. В норме оптимальная частота стимуляции для выявления максимальной реакции усвоения лежит в области собственных частот ЭЭГ, составляя 8-20 Гц. Амплитуда потенциалов при реакции усвоения не превышает обычно 50 мкВ и чаще всего не превосходит амплитуду спонтанной доминирующей активности (рис. 1). Лучше всего реакция усвоения ритма выражена в затылочных отделах, что, очевидно, обусловлено соответствующей проекцией зрительного анализатора, нормальная реакция усвоения ритма прекращается не позднее чем через 0,2-0,5 с по прекращении стимуляции.
Характерной особенностью мозга при эпилепсии является повышенная склонность к реакциям возбуждения и синхронизации нейронной активности. В связи с этим на определенных, индивидуальных для каждого обследуемого частотах мозг больного эпилепсией дает гиперсинхронные высокоамплитудные ответы, называемые иногда фотопароксизмальными реакциями. Вовлекаясь как бы по механизму резонанса в ритмическую активность, ответы на ритмическую стимуляцию в ряде случаев возрастают по амплитуде, приобретают сложную форму спайков, острых волн, комплексов спайк-волна и других эпилептических феноменов (рис. 2).
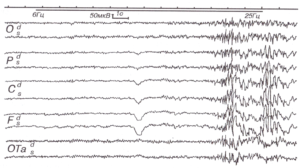
Фоновая ЭЭГ в пределах нормы. При нарастающей по частоте от 6 до 25 Гц световой ритмической стимуляции наблюдается увеличение амплитуды ответов на частоте 20 Гц с развитием генерализованных разрядов спайков, острых волн и комплексов спайк-волна.
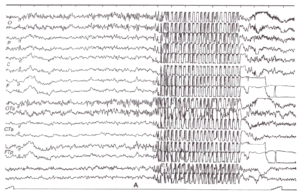
Наблюдавшиеся в течение одного исследования абсансы с генерализованными билатерально-синхронными комплексами спайк-волна в ответ на прерывистую световую стимуляцию (а) и на закрывание глаз (б). На рис. 45 (б) непосредственно перед эпилептическим разрядом виден артефакт движения закрывания глаз.
В некоторых случаях электрическая активность мозга при эпилепсии под влиянием мелькающего света приобретает авторитмический характер самоподдерживающегося эпилептического разряда независимо от частоты стимуляции, вызвавшей его. Разряд эпилептической активности может продолжаться после прекращения стимуляции и иногда переходить в малый или большой клинический эпилептический припадок. Такого рода эпилептические приступы называются фотогенными. У некоторых больных фотогенные приступы сочетаются с возникновением абсансов на закрывание глаз (рис. 3).
Наиболее характерной формой реакции на фотостимуляцию при эпилепсии является фотопароксизмальный ответ (нерекомендуемый синоним — «фотоконвульсивный ответ»). Он характеризуется появлением в ответ на ритмический мелькающий свет генерализованных, обычно билатерально-синхронных комплексов спайк-волна, множественные спайки-волна, спайков и острых волн. Их существенной особенностью является продолжение за пределы времени непосредственного стимула. Нередко эта электроэнцефалографическая активность сопровождается нарушением сознания, симметричными миоклоническими подергиваниями мышц лица, головы и рук, иногда переходящими в общий судорожный припадок (см. рис. 2).
Эту активность следует отличать от фотомиогенного ответа (нерекомендуемый синоним — «фотомиоклонический ответ»), представляющего собой появление в тех же условиях стимуляции повторяющихся пачек мышечных спайков преимущественно в передних отведениях, отражающих частые миоклонические подергивания мышц, в основном глаз и век, иногда с более широким вовлечением мускулатуры головы и шеи. Такая активность наблюдается у части здоровых испытуемых и при некоторых неврологических заболеваниях, не имеющих отношения к эпилепсии. Эта активность, в отличие от фотопароксизмального ответа, обрывается одномоментно с прекращением фотостимуляции.
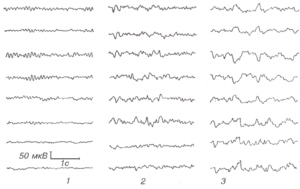
1— до гипервентиляции; 2 — 1,5 мин гипервентиляции; 3 — 3 мин гипервентиляции. Замедление и увеличение амплитуды колебаний.
Гипервентиляция
➥ Более подробно читайте статью: Гипервентиляция
В 1924 г. О.Foerster3 показал, что интенсивное глубокое дыхание в течение нескольких минут провоцирует у больных эпилепсией появление ауры или развернутого эпилептического приступа. С введением в клиническую практику метода электроэнцефалографии было выявлено, что у большого числа больных эпилепсией гипервентиляция уже в первые минуты приводит к появлению и усилению эпилептиформной активности с высокоамплитудными медленными и острыми волнами, комплексами спайк-волна, усилению и генерализации локальных эпилептических проявлений. Обследования здоровых людей показали различный характер ответов мозга на гипервентиляцию в зависимости от возраста. У детей моложе 12-15 лет гипервентиляция уже к концу 1-й минуты закономерно приводит к замедлению ЭЭГ, нарастающему в процессе дальнейшей гипервентиляции, одновременно с увеличением амплитуды колебаний (рис. 4). Эффект гиперсинхронизации ЭЭГ в процессе гипервентиляции выражен тем отчетливее, чем моложе обследуемый4. У здоровых взрослых ЭЭГ оказывается значительно более резистентной к гипервентиляции; увеличение амплитуды с падением частоты наблюдается редко и при гипервентиляции, значительно превышающей по длительности 3 мин.5 В большинстве случаев на ЭЭГ взрослых при гипервентиляции визуальная оценка не выявляет значительных изменений (рис. 5), за исключением небольшого увеличения амплитуды основного ритма.

Обозначения те же, что на рис. 4
Эффект гипервентиляции связан с церебральной гипоксией, развивающейся вследствие рефлекторного спазма артериол и уменьшения мозгового кровотока в ответ на снижение содержания СО2 в крови67.
Экспериментальные данные показывают, что гипоксия приводит к деполяризации мембраны нейронов, повышению их возбудимости и общему деполяризационному сдвигу в коре, с чем и связано провоцирование патологической активности при эпилепсии8.
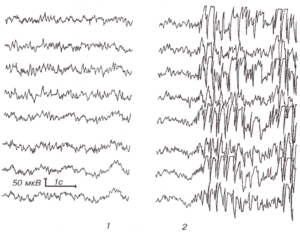
1 — фоновая ЭЭГ. На фоне диффузной дезорганизации регистрируются одиночные и групповые заостренные волны в частоте α, β и θ. Умеренные диффузные изменения с признаками негрубого снижения порога судорожной готовности; 2 — ЭЭГ при гипервентиляции. Возникновение генерализованной активности спайков, множественных спайков, спайк-волна с переходом в припадок атипичный абсанс.
Таким образом, применение гипервентиляции во время записи ЭЭГ позволяет выявить скрытую эпилептическую активность, определить локализацию эпилептического фокуса и в некоторых случаях уточнить характер эпилептических приступов (рис. 6). Обычно используют также комбинированные способы провокации, в частности дают световую ритмическую стимуляцию непосредственно по окончании 3-минутной гипервентиляции. Комбинация световых мельканий с повышенной вследствие гипервентиляции возбудимостью мозга облегчает выявление пароксизмальной активности.
Следует отметить, что у детей до 15-16 лет появление регулярной медленной высокоамплитудной генерализованной активности при гипервентиляции является нормой. Такая же реакция может наблюдаться у молодых (до 30 лет) взрослых. Появление у взрослых при гипервентиляции билатерально-синхронных медленных волн, не сочетающихся с острыми волнами и не имеющих характера вспышек гиперсинхронной активности, не свидетельствует об эпилептическом заболевании и может быть показателем дисфункции стволовых систем и вегетативной нервной системы9.
Появлению эпилептической активности на ЭЭГ способствует и так называемая темновая адаптация. При соблюдении всех необходимых правил регистрации ЭЭГ эта методика является стандартной и применяется у всех обследуемых. Она заключается в непрерывной регистрации ЭЭГ у обследуемого, находящегося в камере с закрытыми глазами, с момента выключения света. Нередко в первые несколько минут этого периода эпилептиформная активность появляется или усиливается.
ЭЭГ во время сна при эпилепсии
➥ Более подробно читайте статью: ЭЭГ сна
Ценным приемом выявления эпилептиформной активности у больных эпилепсией является регистрация ЭЭГ во время ночного сна. Эпилептические проявления активируются во время медленного сна (II-IV стадии) и подавляются при I парадоксальной стадии. Развитию эпилептических проявлений во время медленного сна способствует, очевидно, физиологическая синхронизация нейронной активности, облегчающая эпилептическую синхронизацию. Дополнительным фактором, облегчающим распространение эпилептической активности во время медленного сна, являются «незанятость» нейронов мозга переработкой афферентной информации и в связи с этим повышенная готовность отвечать реакцией возбуждения на импульсацию, приходящую от других систем мозга, вовлеченных в эпилептическую активность10 (Speckmann E.J., Caspers Н., 1973, Steriade М., 1993).
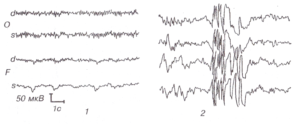
Эпилепсия с ночными генерализованными припадками. 1 — ЭЭГ бодрствования в пределах нормы; 2 — III стадия сна. Разряд спайков, комплексов спайк-волна и полифазных волн.
Анализ ЭЭГ во время сна позволяет обнаружить эпилептиформную активность у большей части больных, у которых в дневное время патологическая активность не выявлялась даже под влиянием обычных методов функциональных нагрузок (рис. 7). Для проведения исследования во время сна в дневное время можно дать больному снотворное в терапевтической дозе11.
Следует сказать, что выявление эпилептиформной активности в ЭЭГ сна требует достаточного опыта и обычно представляет определенные трудности. Это обусловлено наличием в ЭЭГ сна в норме вспышкообразных феноменов — острых вертексных переходных потенциалов и К-комплексов, которые могут напоминать эпилептиформные потенциалы. Высокоамплитудные веретена сна также формально соответствуют критериям острых волн. В связи с этим оценку ЭЭГ следует проводить в контексте всей полиграммы сна, памятуя о приуроченности упомянутых феноменов к определенным стадиям. Дополнительную трудность вносит то, что механизмы генерации упомянутых нормальных сонных феноменов тесно связаны с мозговыми синхронизующими системами, участвующими в эпилептогенезе при патологии, что, в частности, проявляется увеличением количества, продолжительности и амплитуды всех трех упомянутых феноменов при эпилепсии, внося дополнительные проблемы интерпретации и дифференциальной диагностики12. Помимо этого, на ЭЭГ сна, особенно в первой стадии, в определенном проценте случаев у вполне здоровых людей могут наблюдаться вспышки острых волн, комплексов спайк-волна частотой 6 Гц, высокоамплитудных вспышек θ-волн13. В связи с этим уверенным критерием эпилепсии при анализе сонной ЭЭГ следует считать обнаружение паттернов эпилептического припадка или разряда эпилептиформной активности. Как указание на эпилептическую природу припадка, развивающегося во сне по типу височного психомоторного автоматизма, можно рассматривать и возникающую в непосредственной связи с ним высокоамплитудную θ-активность. Следует отметить, что в этом случае возникают трудности дифференциации с сомнамбулическими приступами. Когда возникает такая проблема, следует провести запись сомнограммы в течение целой ночи для оценки характеристик сна и, если возникнет приступ, активности в ЭЭГ, непосредственно ему предшествующей. При сомнамбулизме наблюдается достоверно большее количество эпох с гиперсинхронной (>150 мкВ) δ-акгивностью, большее отношение времени гиперсинхронной δ-активности к общему времени III-IV стадий, большее число прерываний стадий III-IV и тенденция к большему относительному времени стадий III-IV . Самому эпизоду сомнамбулизма непосредственно предшествует и его сопровождает вспышка гиперсинхронной δ-активности14, в то время как эпилептическому психомоторному приступу соответствует вспышка θ-активности.
Провокацию эпилептических разрядов на ЭЭГ можно получить также депривацией сна в течение одной или двух ночей. Эффект в данном случае обусловлен тем, что лишение сна приводит к повышению синхронизации на ЭЭГ, а это является, как указывалось, фактором, благоприятствующим развитию эпилептических потенциалов в мозге.
Использование судорожных препаратов с диагностическими целями при медикаментозном лечении у больных с эпилепсией или с подозрением на нее категорически противопоказано. В связи с совершенствованием современных методов диагностики, в частности с использованием ЭЭГ-видеомониторинга, а также методов функциональной нейровизуализации однофотонной эмиссионной и позитронно-эмиссионной компьютерной томографии, применение с диагностическими целями судорожных препаратов практически полностью исключено и из нейрохирургической эпилептологической практики.
Мозг больного эпилепсией обладает сниженными гомеостатическими возможностями, что отражается в существенно большей изменчивости и непостоянстве характера ЭЭГ по сравнению с нормой. В связи с этим полезными являются повторные исследования ЭЭГ у одного и того же больного в различные периоды суток, поскольку изменения ЭЭГ нередко связаны с биологическими циклами. В частности, выраженность эпилептических проявлений зависит от уровня сахара в крови, в связи с чем у некоторых больных вероятность обнаружения пароксизмальных изменений натощак выше. При оценке ЭЭГ необходимо учитывать проводимую терапию, поскольку применение противосудорожной терапии в существенной мере нормализует ЭЭГ даже в случаях малой клинической эффективности.
Дифференциальная диагностика эпилептических и неэпилептических припадков
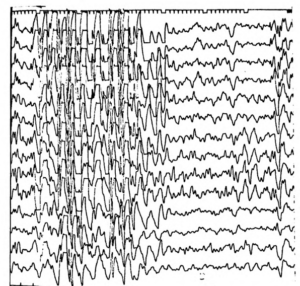
вспышки генерализованной пик-волновой активности частотой от 2,5 до 4-5 в сек. (обычно 3 Гц - типичные абсансы).
Если оставить в стороне приступообразные нарушения соматического происхождения, то основную дифференциально-диагностическую проблему составляют приступы, которые условно можно разделить на вегетативные и психогенные припадки, хотя разделение их нечетко и оба типа включают, как правило, компоненты того и другого. Из вегетативных припадков наиболее часто вопрос о возможности эпилепсии возникает в связи с синкопами.
Более подробно в статьях:
ЭЭГ в диагностике эпилепсии
Идиопатические формы эпилепсий
Детская абсанс эпилепсия
➥Основная статья: Эпилепсия с пикнолептическими абсансами детского возраста и юношеская эпилепсия с абсансами
Абсансы – разновидность генерализованных бессудорожных приступов, характеризующаяся высокой частотой и короткой продолжительностью пароксизмов с выключением сознания и наличием на ЭЭГ специфического паттерна – генерализованной пик-волновой активности с частотой 3 Гц. Дебют абсансов при детской абсанс эпилепсии (ДАЭ) наблюдается в возрастном интервале от 2 до 9 лет, составляя в среднем 5,3 лет. Возрастной пик манифестации – 4-6 лет, с преобладанием по полу девочек. Клинически абсансы характеризуются внезапным коротким выключением (или значительным снижением уровня) сознания с отсутствием или минимальными моторными феноменами.
Факторы, провоцирующие учащение абсансов: гипервентиляция; депривация сна; фотостимуляция; напряженная умственная деятельность или, наоборот, расслабленное, пассивное состояние.
Юношеская абсанс эпилепсия
Юношеская абсанс эпилепсия (ЮАЭ) – разновидность идиопатической генерализованной эпилепсии, характеризующаяся основным видом приступов -абсансами, дебютирующими в пубертатном периоде с высокой вероятностью присоединения ГСП и характерными ЭЭГ изменениями в виде генерализованной пик-волновой активности с частотой 3 Гц и более. Дебют абсансов при ЮАЭ варьирует от 9 до 21 года, в среднем 12,5 лет. У значительного большинства больных (75%) абсансы начинаются в сравнительно коротком временном промежутке – 9-13 лет. Важной особенностью ЮАЗ является частый дебют заболевания с ГСП – 40% случаев В отличие от ДАЭ, гипервентиляция провоцирует возникновения абсансов не более чем у 10% больных ЮАЭ. ГСП у 20% больных провоцируются депривацией сна. При ЭЭГ исследовании в межприступном периоде результаты, близкие к норме, констатируются у 25% пациентов. Основным ЭЭГ паттерном является генерализованная пик-волновая активность с частотой 3 Гц и более (4-5 в сек.), носящая преимущественно симметричный и билатеральносинхронный характер.
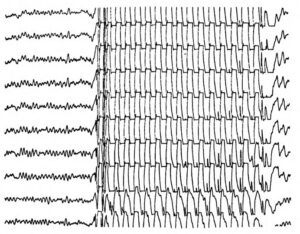
Выражен первично генерализованный эпилептиформный паттерн в виде комплексов спайк медленная волна, частотой 3 в сек.
Фотосенситивная эпилепсия. Миоклония век с абсансами (с-м Дживонса)
Миоклония век с абсансами (МВА) — редкое заболевание, которое начинается в детском возрасте и характеризуется наличием у пациентов изолированных миоклоний век в сочетании с короткими абсансами с заведением глазных яблок и фотосенситивным характером приступов.
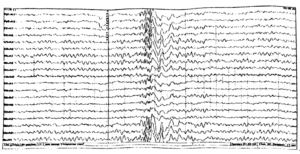
наблюдаемые при фотосенситивных эпилепсиях, в частности и при с-ме Дживонса. Эпилептиформная активность спровоцирована закрыванием глаз. Эпилептиформная активность имеет вид полиспайк-медленная волна, что характерно для группы миоклонических эпилепсий
Эпилепсия с изолированными генерализованными судорожными приступами
Эпилепсия с изолированными генерализованными судорожными приступами (ГСП) определяется как синдром идиопатической генерализованной эпилепсии, проявляющийся единственным видом приступов первично-генерализованными тонико-клоническими судорожными пароксизмами при отсутствии ауры и четкого фокуса на ЭЭГ. Дебют заболевания наблюдается в очень широком возрастном диапазоне: от 1 до 30 лет с максимум в пубертатном периоде (средний -13,5 лет). Клинически ГСП проявляются внезапным (без ауры) выключением сознания с падением пациентов, судорогами, заведением глазных яблок, расширением зрачков. Сначала наступает короткая тоническая фаза, переходящая в более длительную клоническую с последующим постприступным оглушением. Продолжительность ГСП составляет от 30 сек до 10 мин (в среднем 3 мин.). Частота приступов невысока – от единичных в год до 1 раза в месяц, без тенденции к серийному и статусному течению. Характерна приуроченность большинства приступов к периоду пробуждения и, реже, засыпания. Наиболее значимый провоцирующий фактор – депривация сна и внезапное насильственное пробуждение. Возможно учащение приступов в перименструальном периоде.
ЭЭГ исследование в межприступном периоде у половины больных (!) может быть в пределах нормы.
Характерна генерализованная пик-волновая активность с частотой от 3 Гц и выше, нередко с амплитудной асимметрией или бифронтальным преобладанием.
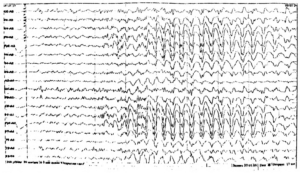
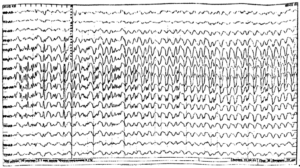
Регистрируется первично генерализованная эпилептиформная активность в виде комплексов острая-медленная волна, выраженная по всем отведениям. Продолжительность припадка составляет более 3 сек., и протекает с потерей пациентом сознания.
Юношеская миоклоническая эпилепсия.
Юношеская миоклоническая эпилепсия (ЮМЭ) – одна из форм идиопатической генерализованной эпилепсии, характеризующаяся дебютом в подростковом возрасте с возникновением массивных билатеральных миоклонических приступов, преимущественно в руках, в период после пробуждения пациентов. ЮМЭ – одна из первых форм эпилепсии с известным генетическим дефектом. Предполагается двулокусная модель наследования (доминантно-рецессивная), причем доминантный ген локализован на коротком плече хромосомы 6.
По данным литературы дебют ЮМЭ варьирует от 7 до 21 года с максимум в возрастном интервале 11-15 лет. Заболевание может начаться в более раннем возрасте с абсансов или ГСП, с последующим присоединением миоклонических приступов в пубертатном периоде. Миоклонические приступы возникают или учащаются в утренние часы, после пробуждения пациента. Основными провоцирующими приступы факторами являются депривация сна и внезапное насильственное пробуждение. Примерно 1/3 больных ЮМЭ (чаще женского пола) обнаруживают фотосенситивность. Эпилептиформная активность на ЭЭГ выявляется у 85% больных в межприступном периоде. Наиболее типична генерализованная быстрая (от 4 Гц и выше) полипик-волновая активность в виде коротких вспышек. Возможно также появление пик-волновой активности 3 Гц.
Доброкачественная детская парциальная эпилепсия с центральновисочными пиками (роландическая эпилепсия) (РЭ)
Идиопатическая парциальная эпилепсия детского возраста, характеризующаяся преимущественно короткими гемифациальными моторными ночными приступами, часто с предшествующей соматосенсорной аурой и типичными изменениями ЭЭГ. Дебют РЗ варьирует в возрастном интервале от 2 до 14 лет. У 20% пациентов судороги могут распространяться с мышц лица на гомолатеральную руку (брахиофациальные приступы) и примерно в 8% случаев вовлекают ногу. Продолжительность приступов от нескольких секунд до 2-3 мин. Частота в среднем 2-4 раза в год. Пароксизмы РЭ “жестко” связаны с ритмом сон-бодрствование. Наиболее типичны ночные приступы, возникающие преимущественно при засыпании и пробуждении.
На ЭЭГ в межприступном периоде обнаруживаются характерные “роландические” пик-волновые комплексы при обязательно сохранной основной активности. Эти комплексы представляют собой медленные дифазные высокоамплитудные пики или острые волны (150 – 300 мкВ), нередко с последующими медленными волнами, общей продолжительностью около 30 мс. Данные комплексы напоминают зубцы ORS ЭКГ. Роландические комплексы обычно локализованы в центральной и лобно-височной области, т.н. сенсомоторной зоне.
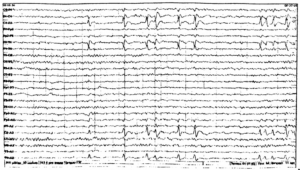
Изменения представлены в виде единичных комплексов типа доброкачественных эпилептиформных разрядов детства (ДЭПД) с преимущественной локализацией в сенсомоторной зоне.
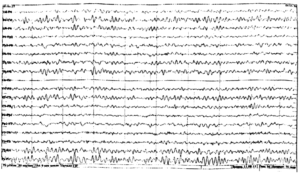
В отведениях сенсомоторной зоны правого полушария регистрируются редуцированные ДЭПД комплексы с переходом на височную область
Идиопатическая парциальная эпилепсия с затылочными пароксизмами.
Идиопатическая парциальная эпилепсия с затылочными пароксизмами (доброкачественная затылочная эпилепсия (ДЗЭ)) – форма идиопатической локализационно-обусловленной эпилепсии детского возраста, характеризующаяся простыми парциальными приступами со зрительными расстройствами и наличием на ЭЭГ специфической пик-волновой активности в затылочных отведениях. Для заболевания характерны простые зрительные галлюцинации, фотопсии, зрительные иллюзии (макро, микропсии). При очаге в затылочной доле часто наблюдается иррадиация возбуждения кпереди (в височную и лобную долю) с появлением сложных структурных галлюцинаций; выключением сознания и возникновением вторично-генерализованных судорожных приступов. Типично возникновение приступов во сне, особенно при пробуждении пациентов. Приступы нередко сопровождаются мигренозными симптомами: головной болью и рвотой.
На ЭЭГ определяется появление высокоамплитудной пик-волновой активности в одном из затылочных отведении или биокципитально независимо. Морфология паттернов напоминает таковую при роландической эпилепсии. Характерно исчезновение эпиактивности при записи ЭЭГ с открытыми глазами
Симптоматические формы эпилепсий
Симптоматическая парциальная эпилепсия
При симптоматических парциальных формах эпилепсии выявляются структурные изменения в коре головного мозга.
Причины, детерминирующие их развитие, многообразны и могут быть представлены двумя основными группами: перинатальными и постнатальными факторами. Среди постнатальных факторов следует отметить нейроинфекции, черепно-мозговые травмы, опухоли коры головного мозга. Дебют приступов при симптоматической парциальной эпилепсии варьирует в широком возрастном диапазоне. Выделяют симптоматические парциальные формы эпилепсии: височную, лобную, теменную и затылочную. Две первых – наиболее частые и составляют до 80% всех случаев.
При нейровизуализации обнаруживаются различные макроструктурные нарушения в головном мозге. Частой находкой при МРТ исследовании является медиальный височный (инцизуральный) склероз; локальное расширение борозд; уменьшение в объеме вовлеченной височной доли; парциальная вентрикуломегалия. Клинически ВЭ проявляется простыми, сложными парциальными, вторично-генерализованными приступами или их сочетанием. ВЭ подразделяют на амигдало-гиппокампальную (палеокортикальную) и латеральную (неокортикальную).
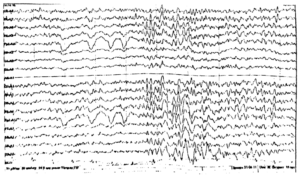
Регистрируется билатеральносинхронная вспышка исходящая из левых височных отведений
Амигдало-гиппокампальная височная эпилепсия
Наблюдается застывание больных с маскообразным лицом, широко раскрытыми ’’изумленными” глазами и уставленным в одну точку взглядом. Характерны различные вегетативные феномены: побледнение лица, расширение зрачков, потливость, тахикардия.
Латеральная височная эпилепсия
Характеризуется нарушениями со стороны слуха и вестибулярного аппарата. При ЭЭГ исследовании наблюдается пик-волновая или чаще стойкая региональная медленноволновая (тета) активность в височных отведениях, обычно с распространением кпереди. У 70% больных выявляется выраженное замедление основной активности фоновой записи. У большинства пациентов с течением времени эпилептическая активность отмечается битемпорально.
Симптоматическая лобная эпилепсия
Проявляется простыми и сложными парциальными приступами, а также, вторично генерализованными пароксизмами.
Формы СЛЭ: моторная, оперкулярная, дорсолатеральная, орбитофронтальная, передняя фронтополярная, цингулярная, исходящая из дополнительной моторной зоны.
Моторные пароксизмы возникают при раздражении передней центральной извилины. Характерны джексоновские приступы, развивающиеся контрлатерально очагу, преимущественно клонические и могут распространяться по типу восходящего (нога-рука-лицо) или нисходящего (лицо-рука-нога) марша. После приступа часто развивается постприступная слабость в конечностях (паралич Тодда). Оперкулярные приступы возникают при раздражении оперкулярной зоны нижней лобной извилины на стыке с височной долей. Проявляются пароксизмами жевательных, сосательных, глотательных движений, причмокиванием, облизыванием, покашливанием; характерна гиперсаливация; ипсилатеральное подергивание мышц лица, нарушение речи или непроизвольная вокализация. Дорсолатеральные приступы возникают при раздражении верхней и нижней лобной извилин. Проявляются адверсивными приступами с насильственным поворотом головы и глаз, обычно контрлатерально очагу раздражения. При вовлечении задних отделов нижней лобной извилины (центр Брока) констатируются пароксизмы моторной афазии. Орбитофронтальные приступы возникают при раздражении орбитальной коры нижней лобной извилины и проявляются разнообразными вегетативновисцеральными феноменами. Характерны эпигастральные, кардиоваскулярные (боли в области сердца, изменение сердечного ритма, артериального давления), респираторные (инспираторная одышка, чувство удушья, сжатия в области шеи, ’’кома” в горле) приступы.
Билатерально-синхронная вспышка эпилептиформной активности из левых лобных отведений, распространяющаяся на лобные отведения контрлатерального полушария
Передние (фронтополярные) приступы
Возникают при раздражении полюса лобных долей. Характеризуются простыми парциальными приступами с нарушением психических функций. Проявляются ощущением внезапного ’’провала мыслей”, “пустоты в голове”, растерянности или, наоборот, насильственным воспоминанием; мучительным, тягостным ощущением необходимости что-то вспомнить.
Цингулярные приступы исходят из передней части поясной извилины медиальных отделов лобных долей. Проявляются сложными, реже простыми парциальными приступами с нарушением поведения и эмоциональной сферы. Возможно появление пароксизмальных дисфорических эпизодов со злобностью, агрессивностью, психомоторным возбуждением.
Приступы, исходящие из дополнительной моторной зоны
Характерно наличие частых, обычно ночных, простых парциальных приступов с альтернирующими гемиконвульсиями, архаическими движениями; приступов с прекращением речи, нечеткими, плохо локализованными чувствительными ощущениями в туловище и конечностях. Парциальные моторные приступы проявляются обычно тоническими судорогами, возникающими то с одной, то с другой стороны, или билатерально (при этом выглядят как генерализованные). Характерно тоническое напряжение с подъемом контралатеральной руки, адверсией головы и глаз (больной как бы смотрит на свою поднятую руку). Характеризуются внезапным пробуждением пациентов, криком, гримасой ужаса, двигательной бурей: размахиванием руками и ногами, боксированием, педалированием (напоминающим езду на велосипеде), тазовыми движениями. ЭЭГ исследование при ЛЭ может показывать следующие результаты: норма, пик-волновая активность; замедление (периодическое ритмическое или продолженное) регионально в лобных, лобно-центральных или лобно-височных отведениях; бифронтальные независимые пик-волновые очаги; вторичная билатеральная синхронизация; региональная фронтальная низкоамплитудная быстрая (бета) активность.
Ограничения возможностей ЭЭГ в эпилептологии
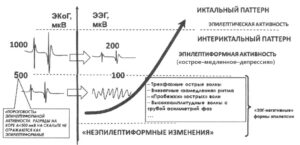
соотношение амплитуды эпилептиформной активности на ЭКоГ и ЭЭГ
В современной эпилептологии парадигма локализации эпилептического очага строится на выявлении ирритативной зоны. Однако следует понимать ограничения, которые содержит сама методика регистрации скальповой ЭЭГ. Во-первых, «разрешающая способность» ЭЭГ в локализации источника патологической активности составляет не менее 3—5 см, то есть практически соизмерима с половиной доли мозга. Увеличение количества электродов, например, переход с системы «10/20» на систему «10/10», не увеличивает «точность» локализации. Во-вторых, при регистрации скальповой ЭЭГ судить о «глубине» расположения источника практически не представляется возможным. Гиперсинхронные разряды, зарождающиеся в глубоких отделах, не всегда отражаются на скальповой ЭЭГ. При «поверхностном» расположении очага эпилептическая активность нейронов зоны коры площадью менее 2 см2 не обладает достаточной мощностью для достижения скальповых электродов. «Волны» ЭЭГ в этом схожи с волнами на поверхности моря. В-третьих, для расчета локализации патологической активности используется дипольная модель генерации биоэлектрической активности. Это не очень грубое, но все же допущение, которое упрощает процессы формирования электрической активности и ее распространение в объемном проводнике, которым является головной мозг. В результате «рассеивания» биоэлектрической активности при переходе через поверхности головы формирование эпилептиформной активности на скальпе носит «пороговый» характер. При одновременной регистрации электрокортикограммы и электроэнцефалограммы было показано, что разрядная активность коры амплитудой менее 500 мкВ не формирует на скальпе эпилептиформные стигматы (рис.). При такой мощности сигнала на ЭЭГ либо возникают трехфазные волны, либо замедления и изменения фазы основной активности. В-четвертых, правила локализации практически строятся на строгом радиальном расположении диполя по отношению к конвекситальной поверхности скальпа. При тангенциальном расположении диполя в силу «разрешающей способности» ЭЭГ определить место истинной инверсии фаз довольно сложно. Это особенно актуально при корковой локализации эпилептогенной зоны, когда относительно не очень мощный источник формирует строго тангенциальный диполь.
В результате указанных ограничений у 20—30 % больных с явной клинической картиной эпилептических приступов на интериктальной ЭЭГ не выявляются типичные эпилептиформные стигматы. Использование иктальной регистрации ЭЭГ также не всегда успешно. При относительно малом размере зоны начала приступа и высокой скорости распространения возбуждения по коре регистрируемая на скальповой ЭЭГ зона может быть более протяженной или даже смещена относительно истинной (корковой) зоны начала приступа. Таким образом, можно выделить особый ряд так называемых «ЭЭГ-негативных» форм эпилепсии.
Наибольшей диагностической эффективностью в эпилептологической ЭЭГ обладает видео-ЭЭГ-мониторинг. При этом методика подразумевает, в первую очередь, регистрацию фазовых состояний при переходе от бодрствования ко сну и «обратно». Длительный мониторинг только ЭЭГ бодрствования мало повышает информативность по сравнению с амбулаторной ЭЭГ. При методически выдержанном мониторинговом исследовании диагностическая точность даже интериктального исследования достигает 85—90 %.
Следует помнить, что регистрируемая эпилептиформная активность сама по себе не является абсолютным основанием для постановки диагноза эпилепсии, а оценивается в комплексе с клиническими проявлениями и данными анамнеза. При скрининговых ЭЭГ исследованиях выявляемость эпилептиформных стигматов может доходить до 20 %. Регистрация эпилептиформной активности не является достаточным условием для постановки диагноза эпилепсии без соответствующей клинической картины. Наличие эпилептиформной активности в отсутствии клиники свидетельствует в том числе и о широких возможностях мозга к компенсации.
И наоборот, у пациентов, много лет страдающих эпилепсией с регулярными приступами, эпилептиформная активность может выявляться на рутинной ЭЭГ примерно в 50 % случаев. Если же речь идет о пациентах, принимающих современные антиэпилептические препараты или имеющих редкие эпилептические приступы (один раз в несколько месяцев), то диагностическая эффективность амбулаторной ЭЭГ резко снижается. В таких случаях многочасовой видео-ЭЭГ-мониторинг с регистрацией сна является основным диагностическим методом.
Читайте также
- Эпилепсия
- Эпилептология
- Эпилептический очаг
- Типы эпилептических припадков
- Изменения ЭЭГ при эпилепсии
- Диагностика эпилепсии по ЭЭГ
- ЭЭГ мониторинг при эпилепсии
Литературные источники
- Александров М. В., Иванов Л. Б., Лытаев С. А. [и др.]. Электроэнцефалография : руководство / под ред. М. В. Александрова. — 3-е изд., перераб. и доп. — СПб.: СпецЛит, 2020. — 224 с.
- Александров М. В., Иванов Л. Б., Лытаев С. А. [и др.]. Общая электроэнцефалография / под ред. М. В. Александрова. — СПб.: Стратегия будущего, 2017. — 128 с.
- Бреже М. Электрическая активность нервной системы : пер. с англ. — М. : Мир, 1979. — 264 с.
- Докукина Т. В., Мисюк Н. Н. Визуальная и компьютерная ЭЭГ в клинической практике. — Минск: Кшгазбор, 2011. — 112 с.
- Зенков Л. Р. Клиническая эпилептология (с элементами нейрофизиологии). – М.: МИА, 2002. – 416 с.
- Зенков Л. Р, Ронкин М. А. Функциональная диагностика нервных болезней: руководство для врачей. — М.: МЕДпресс-информ, 2010. — 488 с.
- Иванов Л. Б. Прикладная компьютерная электроэнцефалография. — М. : МБН, 2004. – 352 с.
- Пенфилд У., Джаспер Г. Эпилепсия и функциональная анатомия головного мозга человека. — М.: Изд. иностр, лит-ры, 1958. — 482 с.
- Русинов В. С., Майоргик В. Е., Гриндель О. М. [и др.]. Клиническая электроэнцефалография / под ред. В. С. Русинова. — М.: Медицина, 1973. — 339 с.
- Niedermeyer E., Lopes da Silwa F. Electroencephalography. Basis, principles, clinical applications related fields. — Philadelphia-Baltimore — NY: Lippincott Williams & Wilkins, 2005. – 1309 p.
Footnotes
- Гриндель О.М. Электроэнцефалограмма при черепно-мозговой травме. В кн.: Клиническая электроэнцефалография. М. Медицина. 1973, с. 213—259.
- Ajmone-Marsan C., Abraham K. Consideration on the use of chronically implanted electrodes in seizure disorders / Confm. neurol., 1966, v. 27, p. 95—110.
- Foerster O. Hyperventilations-Epilepsie / Zbl. ges. Neurol. Psychiat., 1924, Bd. 38, s. 289-293.
- Barnes T.C., Amoroso M.D. The effect of age of the human brain on the electroencephalogram during hyperventilation / Anat. Rec., 1947, v. 99, p.622—624.
- Stoddart J.C. Electroencephalographic activity during voluntary controlled alveolar hyperventilation / Brit. J. Anaesth., 1967, v. 39, p. 2—10.
- Яруллин X. X. Клиническая реоэнцефалография. Л. 1967.
- Stoddart J.C. Electroencephalographic activity during voluntary controlled alveolar hyperventilation / Brit. J. Anaesth., 1967, v. 39, p. 2—10.
- Окуджава В.М. Основные нейрофизиологические механизмы эпилептической активности. Тбилиси, «Ганатлеба». 1969.
- Drake M.E. Paroxysmal hyperventilation responses in the adult Electroencephalogram I Clin. Electroencephalogr. 1986, v. 17, №2, p. 61-65.
- Speckmann E.J., Caspers Н. Neurophysiolgishe grundlagen der Provokationsme-toden in der Elektroenzephalographie / Z. EEG-EMG., 1973, p. 157—167.
- Егорова И.С. Электроэнцефалография. – М.: Медицина, 1973, 296 с.
- Steriade M. Sleep oscillations in corticothalamic neuronal networks and their development into self-sustained paroxysmal activity / Rom. J. Neurol, psychiat., 1993, v. 31, p. 151-161.
- Santamaria J., Chiappa K.H. The EEG of drowsiness in normal adults / J. Clin. Neurophysiol., 1987, v. 4, p. 327-382.
- Blatt L, Peled R., Gadoth N., Lavie P. The value of sleep recording in evaluating somnambulism in young adults / Electroencephalography and clinical Neurophysiology., 1991, v. 78, p. 407—412.