Предобработка
➥ Основная статья: Предобработка ЭЭГ
На этапе предварительной обработки (англ. preprocessing) с полученным сигналом проводится ряд манипуляций, которые помогают преобразовать необработанные данные в формат, более подходящий для дальнейшей обработки и анализа ЭЭГ. При этом следует учитывать, что подходы к предварительной обработке ЭЭГ не стандартизированы и вы можете сами выбирать способы преобразования в зависимости от целей вашего исследования.
Изменение формата данных
Для предобработки можно изменять формат данных или импортировать данные (англ. importing data), например, если вы собираетесь анализировать сигнал с помощью программного обеспечения на основе Python, а ваш изначальный формат EDF, то для работы с данным ПО будет необходимо конвертировать его в формат ACII.
Понижение частоты дискретизации
Понижение частоты дискретизации (англ. downsampling) обычно выполняется, когда вы хотите сэкономить память и время обработки сигнала. Выбор частоты дискретизации должен определяться целью вашего исследования. Если цель – это охарактеризовать компоненты потенциала, связанного с событием (ERP), то частота дискретизации 250 Гц может быть более чем достаточной. Если ваше исследование направлено на характеристику высокочастотных колебаний в диапазоне 30–100 Гц, то желательно использовать частоту дискретизации 1000 Гц или даже 2000 Гц.
Cегментация
Под сегментацией (англ. segmentation) понимается процедура, при которой из непрерывного сигнала ЭЭГ извлекаются определенные временные промежутки. Эти временные окна называются “эпохами” и обычно фиксируются во времени в отношении интересующего вас события, например, визуального стимула.
Удаление шумов и артефактов
- Производить удаление шумов и артефактов можно, применяя для этого фильтры, такие как фильтр верхних частот, для удаления составляющих постоянного тока сигналов (нижних частот), а также дрейфов (обычно достаточно частоты среза 1 Гц). Фильтр нижних частот также может применяться для удаления высокочастотных компонентов.
- Во время записи ЭЭГ мы можем получить артефакты, вызванные электродами: их плохим контактом с кожей головы, повреждением, наличием высокого импеданса. Данную проблему можно решить удалением плохого канала (англ. removing bad channels) и последующей интерполяцией (англ. interpolation) (т.е. заменой плохих фрагментов хорошими за счет данных с других каналов).
- Для очистки сигналов можно использовать коррекцию артефактов (англ. artifact correction), например, электроокулограммы (EOG), что можно сделать применяя такие методы как метод главных компонент (PCA),1 линейного дискриминантного анализа (LDA), метод независимых компонент (ICA)23 и др. Применение этих методов анализа также снижает размерность сигнала, что позволяет уменьшить количество переменных, отсекая лишние данные.
Ремонтаж
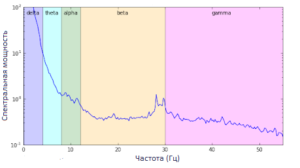
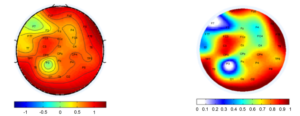
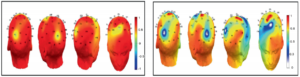
Ремонтаж (англ. remonage, re-referencing, reformatting) – изменение референса в оффлайн режиме после проведения записи. Идея ремонтажа заключается в том, чтобы выразить напряжение в каналах скальпа ЭЭГ по отношению к другому, новому эталону. Цифровые системы позволяют переформатировать монтажи, что может способствовать, например, уменьшению шума или увеличению амплитуды для оптимального отображения активности мозга в момент интерпретации сигнала. 45 Технически, признак представляет собой отличительное свойство, узнаваемое измерение и функциональную компоненту, полученную из фрагмента паттерна. Извлечение признаков (англ. feature extraction) предназначено для минимизации потерь важной информации, заложенной в сигнал, что позволяет выделить все данные, которые могут иметь значение для постановки диагноза или вынесения заключения. То есть мы создаем новый набор признаков, который фиксирует большую часть полезной информации. Кроме того, на этом этапе сокращают объем информации, необходимой для точного описания огромного набора данных т.е. снижается размерность, что позволяет уменьшить время проведения анализа ЭЭГ, не искажая конечный результат. Сегодня, благодаря компьютерам, мы можем применять сложные алгоритмы автоматической обработки, которые позволяют извлекать «скрытую» информацию из сигналов ЭЭГ. Для этого мы можем применять несколько методов, таких как функции временной области (среднее значение, стандартное отклонение, энтропия),67 функции частотной и частотно-временной области (преобразование Фурье, вейвлет-преобразование и т. д.)89 статистические методы, такие как PCA, LDA, ICA.1011 Следующий шаг, называемый отбор признаков (англ. feature selection), обычно, выделяется как необязательный и используется в случае, когда мы имеем большое количество признаков, и хотим изучить те, которые более актуальны для нашего исследования. Выбор признаков предназначен для фильтрации нерелевантных или избыточных признаков из вашего набора данных. Ключевое различие между отбором признаков и извлечением состоит в том, что при отборе сохраняется подмножество исходных признаков, а при извлечении признаков создаются новые. Представьте, что мы хотим найти возможные различия на ЭЭГ в двух разных состояниях: расслабленном и напряженном. Мы можем применить этап выбора признаков, чтобы найти среди нашего большого количества признаков те, которые наиболее различают эти два условия. Для реализации этого этапа применяют, например, генетический алгоритм (англ. genetic algorithm),1213 квантование вектора обучения (англ. learning vector quantization) или его расширенную версию distinction sensitive learning vector quantization (DSLVQ).1415 ➥ Основная статья: Методы классификации сигналов ЭЭГ Стоит отметить, что конечной целью обработки ЭЭГ-сигналов является их классификация (англ. сlassification) в соответствии с их свойствами. Используя методы машинного обучения, мы можем обучить классификатор распознавать среди наших признаков, какие из них принадлежат к одному классу (или состоянию, т. е. расслабленному) или к другому (т. е. напряженному). Для этого возможно применение искусственных нейронных сетей,16 линейный дискриминантный анализ, метод опорных векторов и метод k-ближайших соседей. Выбор метода классификации напрямую зависит от свойств анализируемых данных и имеющихся вычислительных мощностей. Так, например, нейронные сети обладают высокой скоростью работы и просты в использовании, но их производительность напрямую зависит от количества нейронов в скрытом слое, т.е. высокопроизводительные нейронные сети достаточно сложны в создании. ➥ Основаная статья: Коннективность мозга Используя результаты корреляционного, когерентного и др. методов анализа можно отражать коннективность (англ. connectivity) или связанность,17 что позволяет выстраивать структуру связей в головном мозге.1819 Это можно применить в изучении коннективности и построении коннектома, т.е. исследованиях, связанных с построением структуры связей в нервной системе организма. Визуализация (англ. visualization) направлена на удобное и понятное для специалиста представление результатов. Это облегчает постановку диагноза, упрощает и уточняет работу аналитика. При работе на данном этапе применяется картирование ЭЭГ. Самым основным методом визуализации данных ЭЭГ является простой график временных рядов. Время устанавливается по горизонтальной оси, а напряжение по вертикальной оси. Слева обычно в столбик отображены задействованные электроды. Еще одним распространенным методом является постороение спектральных графиков (спектрограмм), основанных на преобразовании Фурье, либо вейвлет преобразовании. Если по нативной ЭЭГ можно лишь констатировать факт изменчивости основного ритма, то на спектрограммах и визуально, и количественно доступно определить за счет каких частотных компонентов это происходит.20 Визуализация изменений активности мозга, также полезна во время выполнения когнитивной работы для обнаружения и отслеживания динамики и сложности функций мозга, понимания скрытых, новых и сложных нейронных паттернов и тенденций в условиях нормальной и когнитивной нагрузки. Что можно сделать при помощи построения 2D топографических круговых карт поля данных, записанных со скальпа, или сферической карты поля ЭЭГ на полуреалистичной 3D модели головы.21 Двумерная визуализация часто используется для установления точных взаимосвязей, позволяющих анализировать детали и проводить точные навигационные и дистанционные измерения. Трехмерная визуализация используется для получения качественной интерпретации, облегчения исследования трехмерного пространства и лучшего понимания функциональной динамики мозговых сетей.Выделение признаков
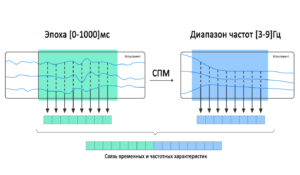
Отбор признаков

Классификация
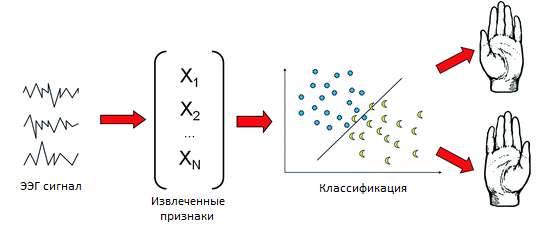
Коннективность
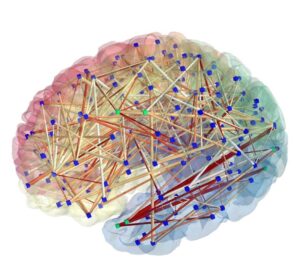
Визуализация
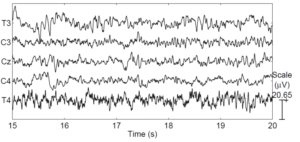
Footnotes