С развитием и внедрением в практику информационных технологий возник вопрос о возможности автоматизации анализа электроэнцефалограмм. В данной статье будут рассмотрены некоторые методы компьютерного анализа и обработки сигналов ЭЭГ.
Когерентный анализ ЭЭГ
➥ Основная статья: Когерентный анализ ЭЭГ
Когерентный анализ (англ. coherence analysis) – это процесс изучения степени синхронизации частотных составляющих ЭЭГ между различными отделами коры головного мозга. Когерентность в целом – количественный показатель, отражающий взаимосвязанность электрических процессов мозга и отражающий корреляцию спектральной мощности ЭЭГ, которая определяется для разных отведений в одном и том же частотном диапазоне1.
Т.о. данный тип анализа позволяет установить взаимосвязь или коннективность отдельных участков коры головного мозга. Физиологически данное явление обусловлено способностью нейронов генерировать разряды синхронно для оптимизации работы при выполнении сложной когнитивной деятельности.
Количественно когерентность отражается с помощью коэффициента когерентности и измеряется между двумя скальповыми отведениями. Значение данного коэффициента может изменяться от 0 до 1 – чем оно выше, тем больше согласованность активности одной области коры с другой.
В условиях нормальной деятельности показатель когерентности увеличивается при решении сложных когнитивных задач. Однако возможно и патологическое изменение данной характеристики. Так, например, данный показатель снижается при патологической дисфункции нейронных сетей (деменция, дислексия, болезнь Альцгеймера) и чрезмерно увеличивается при уменьшении или повреждении мозолистого тела, т.е. является компенсаторным механизмом2.
Т.о. когерентный анализ позволяет получить информацию о стабильности взаимосвязи между отдельными участками мозга и оценить статистическую связь между соответствующими частотными компонентами двух электрофизиологических процессов3.
К преимуществам данного метода анализа можно отнести его независимость от амплитуды колебания сигналов различных участков головного мозга и высокую чувствительность. Однако стоит отметить, что когерентный анализ не вполне точно отражает форму сигнала и временную связь между процессами, т.к. данный метод исследует синхронность частотных составляющих, не исправляя форму сигнала и не касаясь временных характеристик4.
На практике для проведения когерентного анализа используется программный комплекс “Энцефалан-ЭЭГ” на базе аппарата “Энцефалан-131-03“. В данном программном обеспечении (далее – ПО) в режиме «Спектральный анализ» расчет функции когерентности производится для всех отведений ЭЭГ относительно любого выбранного отведения. Обработка ЭЭГ ведется по эпохам (т.е. отдельным временным промежуткам), с накоплением результатов. В результате расчета формируются графики когерентности, и одновременно с ними показываются топографические карты, отражающие распределение средних значений функции когерентности в выбранных частотных диапазонах.
Альтернативой является программа BESA Research от компании Megis Software GmbH, которая позволяет вычислять когерентность событий на частотно-временной шкале.
WinEEG – программный комплекс для всестороннего анализа ЭЭГ – включает в себя в т.ч. и когерентный анализ, проводимый в автоматическом режиме для любой части записанной ЭЭГ.
Еще одним вариантом является комплекс “Неврополиграф”, обладающий рядом функций, в число которых входит проведение когерентного анализа с одновременным картированием когерентности, причем онлайн – т.е. в процессе снятия ЭЭГ.
Кроме того возможно использование системы Brainsys для автоматического анализа ЭЭГ с последующим формированием схемы межполушарных и внутриполушарных связей.
Преобразование Фурье в ЭЭГ
➥ Основнаая статья: Преобразование Фурье, как метод анализа ЭЭГ-сигналов
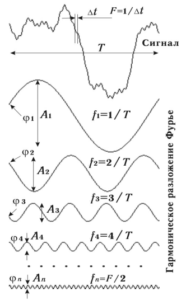
Среди прочих методов для анализа биоэлектрической активности головного мозга используется т.н. спектральный метод, подразумевающий описание распределения мощности по частотным составляющим. Т.о. у исследователя появляется возможность определить, на какой частоте волны имеют наибольшую мощность. В анализе ЭЭГ это позволяет выделить наиболее информативные частоты с последующим анализом их амплитуд с целью выявления патологической активности.
Математической основой спектрального анализа является преобразование Фурье (Fourier transform, FT)5, которое рассматривает сигнал как сумму гармонических составляющих возрастающей частоты. Сущность метода состоит в следующем: любой электромагнитный сигнал является, по сути, изменением напряжения с определенной частотой. Если взять производную по частоте от базовой синусоиды, то мы получим те самые гармонические составляющие или гармоники. Это действие и называется разложением сигнала на гармонические составляющие.
Использующиеся на практике сигналы являются дискретными, т.е. состоящими из огромного числа отдельных величин. Соответственно, после регистрации сигнала возможно его разложение на отдельные составляющие в соответствии с частотой оцифровки.
Таким образом получаются важные для дальнейшей обработки характеристики – зависимости амплитуд и начальных фаз от частоты. Ключевым свойством является обратимость данного процесса – из отдельных гармоник возможен обратный переход к изначальному сигналу без потери информации.
В практическом плане использование данного метода позволяет очистить полученный сигнал от шумов и помех и выделить наиболее значимые для постановки диагноза компоненты. Применение преобразования Фурье в компьютерном анализе позволяет автоматизировать наблюдение за процессами, имеющими клиническое значение, например, регистрировать глубину анестезии путем регистрации ЭЭГ-ритмов, сигнализирующих о наступлении фазы глубокого сна.
Стоит отметить, что преобразование Фурье, несмотря на относительную простоту и обратимость, обладает рядом недостатков. Так, например, возможно возникновение спектральной утечки – явления, сущность которого состоит в распределении мощности спектральных составляющих по диапазону частот. Это приводит к появлению новых частот, которых нет в изначальном сигнале, т.е. мощности реальных частот “просачиваются” в другие диапазоны. Кроме того, преобразование Фурье “сглаживает” сигнал, что приводит к снижению разрешения и исчезновению деталей, которые могут быть важны для исследования.
Другим недостатком преобразования является невозможность работы с нестационарными сигналами – т.е. сигналами, свойства которых сильно изменяются во времени, т.к. преобразование Фурье показывает сам факт наличия в сигнале той или иной частоты, но не привязывает эту частоту к какому-то конкретному отрезку времени.
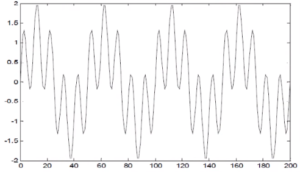
Так, например, сигнал на рисунке 2, содержащий в себе частоты в 10 и 50 Гц, которые присутствуют в сигнале одновременно, после преобразования Фурье будет иметь вид, представленный на рисунке 3.
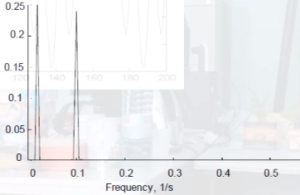
При этом другой сигнал, также имеющий частоты в 10 и 50 Гц, но расположенные последовательно (рисунок 4), после преобразования Фурье будет иметь вид крайне схожий с предыдущим сигналом (рисунок 5).
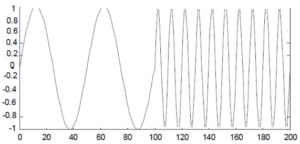
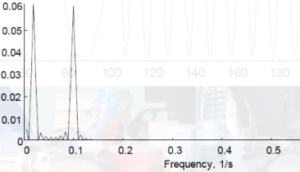
Данный недостаток исправляется вейвлет-преобразованием, о котором речь пойдет дальше.
На практике данный метод применяется в большинстве доступного ПО – комплексы BESA, Neurotravel и “Энцефалан”, программы Brainsys, NeoRec, EDFbrowser и WinEEG используют данный метод для проведения спектрального анализа и очистки регистрируемых сигналов.
“Энцефалан” , который позволяет представить результаты анализа полученных сигналов в виде графиков спектральной плотности мощности, амплитудных спектров, топографических карт или различных количественных показателей в табличном виде.
Вейвлет анализ ЭЭГ
➥ Основная статья Вейвлет-преобразование
Вейвлет-анализ6 ЭЭГ основан на таких математических понятиях, как вейвлет и вейвлет-преобразование.
Вейвлет ( англ. wavelet — небольшая волна) – математическая функция, делающая возможным анализ различных частотных компонент полученных в результате снятия ЭЭГ данных, за счет привязки спектра сигнала ко времени.
Вейвлет-преобразование – преобразование сигнала с помощью вейвлета, перевод его из временного представления в частотно-временное. Поясним. Большая часть сигналов представлена во временной области, т.е. сигнал изображен как график зависимости частоты от времени, что и представлено на иллюстрации (рис. 6).
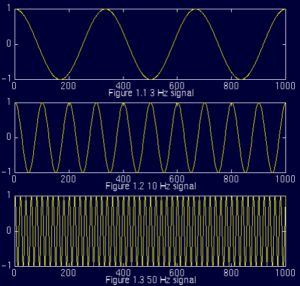
Другое их название – амплитудно-временное представление сигнала, т.к. они иллюстрируют изменение амплитуды сигнала во времени.
Однако зачастую для анализа требуется информация о частотных (спектральных) характеристиках сигнала, т.е. о наличии в полученном сигнале тех или иных частот. Для получения этой информации требуется перевод сигнала из амплитудно-временного в частотное представление. Именно с этой целью применяется преобразование Фурье и вейвлет-анализ.
Если рассматривать вейвлет-преобразование применительно к иллюстрации выше, то мы получим следующий результат, приведенный на рисунке 7.
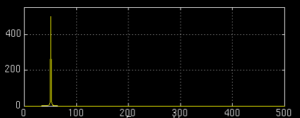
Стоит отметить, что здесь приведено преобразование только третьего сигнала с частотой 50 Гц. Данная иллюстрация показывает, что на исследуемом фрагменте времени (ось Оу) в течение 400 мс определяется только один сигнал – с частотой 50 Гц (ось Ох).
Другим примером, иллюстрирующим работу данного метода является рисунок 8.
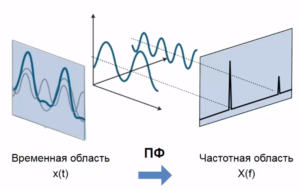
Как мы видим, сигнал, расположенный в частотно-временной области, проецируется отдельно во временную и отдельно в частотные области.
Отличия между преобразованием Фурье и вейвлет-анализом носят преимущественно математический характер. Существенным различием на практике являются следующие два факта:
- Вейвлет-преобразование не осуществляется для отрицательных частот;
- Вейвлет-преобразование дает возможность масштабировать результаты, т.к. вычисляется для каждой спектральной компоненты
В анализе ЭЭГ вейвлет-преобразование может быть проиллюстрировано следующим примером.
На рисунке 9 изображена ЭЭГ здорового человека, которая представлена в виде графика зависимости амплитуды от времени. Однако данный график не дает информации о спектральных характеристиках сигнала.
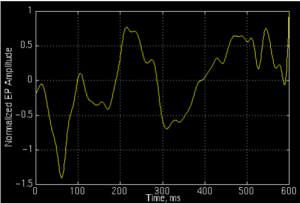
Если подвергнуть его вейвлет-преобразованию, мы получим изображение того же самого сигнала, представленного в виде трехмерного графика, который иллюстрирует не только распределение амплитуды сигнала во времени, как первый, а связывает амплитуду, время и частоту. То есть данный график дает возможность определить, в какой конкретно момент времени какая конкретно частота возникла и как долго она существовала.
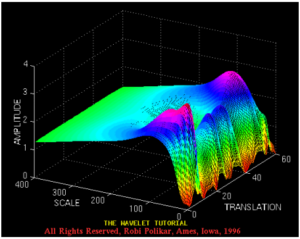
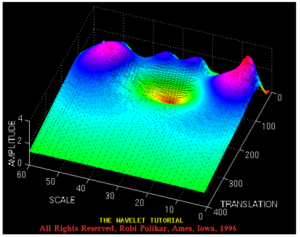
Другим представлением результатов вейвлет-преобразования может служить следующая серия иллюстраций (рисунки 12 и 13)

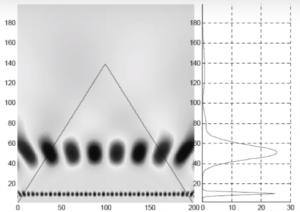
На рисунке 12 представлен стационарный сигнал, т.е. сигнал, свойства которого повторяются во времени. Данный сигнал состоит из двух совмещенных сигналов частотой 10 и 50 Гц. После того, как мы подвергли его вейвлет-преобразованию, мы получили рисунок 13, где в правой части представлены спектральные характеристики сигнала (т.е. составляющие какой частоты и в течение какого времени присутствуют в анализируемом сигнале), а в левой – их распределение (где длина обозначает амплитуду, положение по оси Y – частоту, а положение по оси Х – момент времени, в который существует волна).
Если же мы проведем вейвлет-анализ для нестационарного сигнала (т.е. сигнала, свойства которого сильно изменяются во времени), то результаты будут сильно отличаться (см. рисунки 14 и 15).

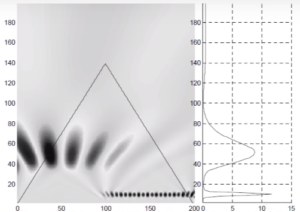
Логика графика такая же, как и в случае со стационарным сигналом, представленным выше. Однако стоит обратить внимание, что левая часть графика существенно отличается, т.к. в момент времени 100 частота сигнала изменилась с 10 Гц на 50 Гц.
Отмечу, что представленные выше примеры относятся к непрерывному вейвлет-преобразованию. Кроме него существует еще и дискретное – более экономное в плане используемых коэффициентов, математических операций и компьютерных мощностей. Однако его отличия лежат в математической плоскости, которая в данной работе не рассматривается.
Вейвлет-анализ используется для исследования нестационарных сигналов (т.е. тех сигналов, изменения характеристик которых нецикличны) и обладает такими важными особенностями, как:
- локализация сигнала во временной и частотной областях одновременно;
- разнообразие выбора базиса, по которому раскладывается сигнал, что позволяет учесть особенности анализируемых данных;
- низкая чувствительность к зашумлению данных;
- возможность изучения локальных особенностей сигнала;
- эффективность анализа коротких временных рядов.
В анализе ЭЭГ вейвлет-преобразование позволяет выделять компоненты, соответствующие ритмам с нужной исследователю частотой, что дает возможность рассматривать их независимо друг от друга и изучать частотные и другие свойства каждой компоненты. Так, например, опубликованы работы, использующие вейвлет-преобразование для исследования реакции нервной системы на воздействие внешнего стимула78.
Однако стоит учитывать, что при проведении вейвлет-анализа возникают амплитудные искажения, которые затрудняют сопоставление вейвлетов различного масштаба и частоты.
Что касается ПО, используемого для проведения данного типа анализа, то в первую очередь стоит упомянуть систему математического моделирования Matlab с пакетом расширений Wavelet-toolbox и сервер ZETLAB.
Корреляционный анализ ЭЭГ
➥ Основная статья: Корреляционный анализ
Корреляционный анализ (ангд. correlation analysi, метод анализа корреляционной синхронности, s, КА) – это метод обработки ЭЭГ, основанный на вычислении коэффициента корреляции, авто- и кросскорреляционных функций.
В данном случае автокорреляция – это анализ участков ЭЭГ одинаковой длительности, относящихся к одному отведению. Кросскорреляция – это, соответственно, анализ участков ЭЭГ одинаковой длительности, относящихся к разным отведениям.
Для установления характеристик связи между переменными находится коэффициент корреляции. В зависимости от свойств анализируемых параметров используется либо коэффициент корреляции Пирсона (если распределение величин близко к нормальному), либо коэффициент корреляции Спирмена (если распределение ненормально). В данном случае под термином “нормальное распределение” подразумевается такой набор показателей, матожидание (ожидаемое среднее значение величины) которого равно 0, а стандартное отклонение равно 19.
Значение коэффициента корреляции Пирсона варьируется от -1 до +1. Чем меньше его значение по модулю, тем меньше степень взаимосвязи между явлениями, т.е. наиболее явно связь прослеживается при коэффициенте корреляции +1 или -1.
Прямая корреляция (коэффициент корреляции больше 0) свидетельствует о синфазности, т.е. нарастающая амплитуда первого сигнала соответствует увеличению амплитуды второго сигнала и наоборот.
Обратная корреляция (коэффициент корреляции меньше 0) – означает, что сигналы противофазны, т.е. нарастающая амплитуда первого сигнала соответствует уменьшению амплитуды второго сигнала и наоборот.
При значении коэффициента корреляции 0 сигналы асинхронны, т.е. изменение одного сигнала никак не затрагивает показатели второго.
Интерпретация коэффициента Спирмена проводится аналогичным образом.
К достоинствам корреляционного анализа ЭЭГ относится:
- простота использования;
- скорость получения результата;
- отсутствие необходимости в приобретении сложного оборудования.
Недостатки корреляционного анализа:
- возможно выявление отчетливой связи лишь между доминирующими фрагментами сигнала;
- улавливание только быстротечных элементов изменения синхронности двух явлений.
Применяется КА для обнаружения смешанных с шумом сигналов с известными свойствами, полученных с электродов, установленных в различных точках головы, для обнаружения повторяющихся событий (например, спайк-волн ЭЭГ сигнала)10.
Суть корреляционного анализа состоит в нахождении взаимно-корреляционной функции, отражающей связь фрагмента обрабатываемого сигнала и эталона сигнала без помех и шумов, что позволяет оценить степень сходства полученных в результате исследования данных и образца. В итоге мы получаем возможность оценить уровень зашумления сигнала или близость его к какому-либо паттерну.
В качестве образца какого-либо ЭЭГ-сигнала используется либо стандартный фрагмент данного сигнала, заранее очищенный от помех и шумов, либо искусственно созданная модель стандартного фрагмента ЭЭГ-сигнала, построенная на основе заранее известных данных о форме и амплитудно-временных характеристик.
Существует несколько способов применения корреляционного анализа ЭЭГ.
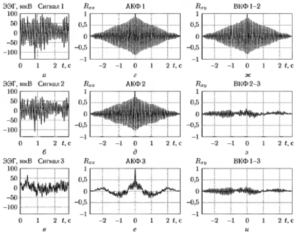
Так, на рисунке 16 приведены фрагменты ЭЭГ под буквами а, б и в. График под буквой г изображает автокорреляционную функцию фрагмента а. Подобная функция графика свидетельствует о том, что сходство двух эпох данного сигнала сходит на ноль относительно медленно. Следовательно, мы можем сделать вывод о периодичности процессов, протекающих в данном отведении, т.к. отдельные его фрагменты достаточно сильно схожи друг с другом. Аналогичные выводы можно сделать и о сигнале на графике б, опираясь на его функцию, обозначенную буквой д.
С другой стороны, график в, автокорреляционная функция которого изображена на рисунке е, изображает хаотический процесс, отдельные фрагменты которого не подобны друг другу. Об этом свидетельствует крайне быстрое затухание его автокорреляционной функции. Т.о. процессы, протекающие в данном отведении, непериодичны, т.к. отдельные фрагменты графика мало схожи друг с другом.
График ж изображает кросс-корреляционную функцию между сигналами а и б. Ее медленное затухание свидетельствует о наличии взаимовлияния фрагментов а и б. График з и график и отражают кросс-корреляционную функцию между сигналами б-в и а-в соответственно. Поскольку затухание графика происходит достаточно быстро, мы можем сделать вывод о том, что между данными отрезками ЭЭГ-сигнала отсутствует существенная взаимосвязь.
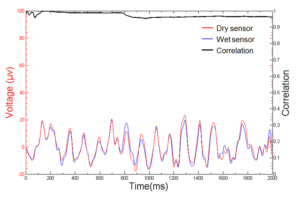
На рисунке 17 мы видим сравнение графиков напряжения при использовании сухих (красный) и влажных (синий) электродов. Степень корреляции результатов представлена в виде графика черного цвета в верхней части изображения.
Корреляционный анализ применительно к исправлению графика ЭЭГ представлен на рисунке 18.
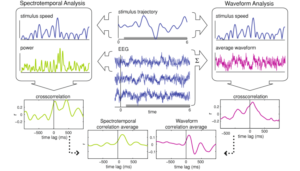
В центре иллюстрации приведено два графика – график воздействия стимула сверху (синий цвет) и фрагмент ЭЭГ снизу (синий цвет).
В левой части изображены графики скорости воздействия стимула (синий цвет) и мощности ЭЭГ (зеленый цвет). Их подвергли кросскорелляционному анализу, результат которого приведен ниже (зеленый цвет). Затем, используя полученные данные о корреляции, был построен исправленный график ЭЭГ-сигнала (зеленый цвет).
В правой части иллюстрации изображены графики скорости воздействия стимула (синий цвет) и средней формы волны (розовый цвет). Последний был получен путем суммации изначальных ЭЭГ-графиков. Их также подвергли кросскорелляционному анализу, результат которого приведен ниже (розовый цвет). Затем, используя полученные данные о корреляции, был построен исправленный график ЭЭГ-сигнала (розовый цвет).
Для проведения корреляционного анализа используется комплекс ПО, поставляемый с электроэнцефалографом “Энцефалан”. Построение автокорреляционных функций позволяет выделить гармонические колебания в случайном процессе. Кросс-корреляционный анализ дает возможность количественно оценить степень сходства процессов, протекающих в разных участках мозга, их связь, общие компоненты и их соотношение, а также временные отношения разных ритмов.
Альтернативой является комплекс “Неврополиграф”, который имеет возможность проводить авто – и кросскорреляционный анализ по заранее загруженным схемам.
Кроме того возможно применение программного комплекса Brainsys, который позволяет вычислять коэффициент корреляции спектров ЭЭГ (как между собой, так и с любыми произвольными параметрами) и картировать распределение корреляции.
Корреляционные методы позволяют более точно локализовать патологический процесс в тех случаях, когда ЭЭГ пораженной и смежной области сходны между собой и практически неотличимы при визуальной оценке.
Метод главных компонент для ЭЭГ
➥ Основная статья: Метод главных компонент
Метод главных компонент (англ. principal component analysis, PCA, преобразование Хотеллинга, дискретное преобразование Кархунена – Лоэва) – это линейное преобразование, которое отображает данные из имеющегося огромного пространства в новой системе координат с меньшей размерностью без потери необходимой для исследования информации11. В данном случае размерность – это количество независимых параметров, необходимых для идентификации точки пространства. Так, например, топологическая карта абсолютно плоского пространства будет иметь размерность равную 2, т.к. для описания любой точки на ней необходимо задать два независимых параметра – координату по Х и координату по Y.
Иными словами, этот метод позволяет обнаружить линейную комбинацию между переменными и избрать наиболее значимые составляющие, понизить размерность, что является его основным достоинством.
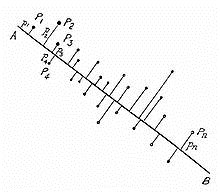
Проиллюстрируем. На рисунке 19 представлено множество точек Pi, расположенных в пространстве с размерностью равной 2 и лежащих на расстоянии pi от прямой АВ. В самом примитивном виде, суть метода заключается в поиске такого положения прямой, чтобы сумма pi2 была минимальной (данная величина иллюстрирует суммарное расстояние от всех точек до прямой)12.
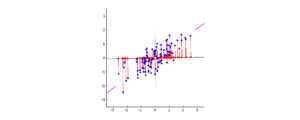
На анимированном рисунке 20 в виде точек изображено множество значений (в случае ЭЭГ это могут быть значения частоты в определенные моменты времени) на координатной плоскости. Задача PCA состоит в нахождении оптимального положения прямой (на иллюстрации обозначено розовыми линиями).
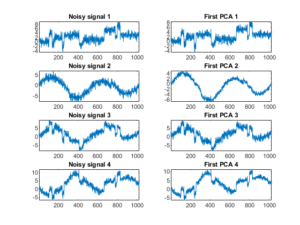
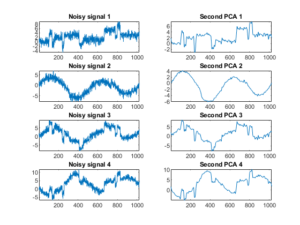
Для ЭЭГ примером может служить рисунки 21 и 22, на которых представлен процесс очистки ЭЭГ сигнала путем проведения PCA. В левой части обоих изображений представлен зашумленный сигнал, в правой – очищенный. При этом на первой иллюстрации исправленные графики – продукт однократной обработки, на второй – двукратной.
Использование данного метода позволяет выделять значимую информацию и подавлять шум на изображении. В анализе ЭЭГ данный метод применяется для удаления помех и артефактов в таких программах как БОСЛАБ, WinEEG, WICA, AWICA, FieldTrip и Brainstorm.
Преимуществами метода главных компонент является:
- снижение размерности;
- изменение базовых функций метода в зависимости от исследуемого ряда и поставленных задач;
- возможна оценка мгновенных частоты и амплитуды периодических компонент исходного временного ряда и их фазы;
- имеется возможность полного или частичного восстановления временного ряда по информативным компонентам, что приводит к выборочной фильтрации или сглаживанию исходного временного ряда13.
Недостатки метода:
- низкая скорость вычислений при работе с большим количеством каналов, поскольку требуется обработка нескольких крупных матриц14;
- нет возможности смысловой интерпретации компонент, т.к. они включают в себя дисперсию от двух и более первоначальных переменных;
- метод применяется для работы только с недискретными данными.
Анализ независимых компонент ЭЭГ
➥ Основаня статья: Метод независимых компонент
Метод независимых компонент (англ. Independent Component Analysis, ICA) – это метод анализа ЭЭГ, основанный на разделении многомерного сигнала на обособленные подкомпоненты, которые статистически независимы друг от друга. Ярким примером является т.н. “Задача о шумной вечеринке” – способность мозга выделять голос собеседника из общего звукового фона. Аналогичным способом возможно использовать данный метод в анализе ЭЭГ – для выделения имеющего значение сигнала из всей совокупности.
В случае ЭЭГ анализ независимых компонент позволяет отделить основные данные от помех, вызванных морганием, движением глаз, сокращениями миокарда и мышечной активностью. По сравнению с вышеописанным РСА, ICA обладает большей эффективностью в отношении сохранения значимой информации об электрической активности.
Метод независимых компонент основан на двух принципах. Первый гласит, что разделяемые сигналы обособлены, т.е. их разделение представляется возможным. Второй гласит, что распределение значений должно отличаться от нормального.
Существует ряд алгоритмов обработки данных по этому методу – Infomax, FastICA, JADE, ядерный независимый компонентный анализ – каждый из которых содержит несколько обязательных частей:
- Центрирование, т.е. вычитание среднего значения из каждой переменной для устранения смещения;
- Снижение размерности с помощью РСА;
- Декорреляция, т.е. приведение к единице дисперсии всех переменных.
С точки зрения математики процесс анализа по методу независимых компонент представляется как работа с матрицей, имеющей Т рядов и N колонок.
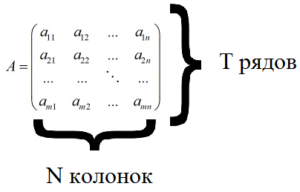
При этом количество рядов совпадает с количеством источников (электродов), а количество колонок – с количеством временных точек, т.е. моментов получения данных. Дальнейший процесс обработки направлен на поиск компонентов матрицы, совокупность которых является пространственным “фильтром” искомой компоненты, т.е. позволяет вычленить искомые данные из смешанного сочетания их. После этого возможно построение графика сигнала, очищенного от помех.
На рисунке 24 представлен результат обработки зашумленного ЭЭГ-сигнала методом ICA.
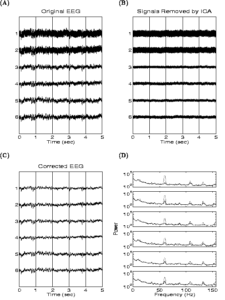
Другим примером приложения метода ICA к анализу ЭЭГ может служить рисунок 25.
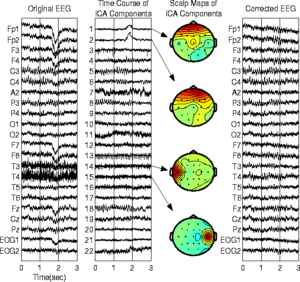
Преимущества метода состоят в следующем:
- Отдельные компоненты (т.е. и помехи, и значимые сигналы) могут находиться в одной пространственной плоскости;
- Отсутствует необходимость в измерении параметров артефактов;
- Снижается нагрузка на оборудование для анализа за счет уменьшения количества каналов;
- Высокая чувствительность к силе сигнала.
Недостатки метода заключаются в:
- Количество источников совпадает с количеством электродов;
- Потребность в большом объеме вычислений.
Т.о. метод ICA позволяет решить задачу слепого разделения источников, лежащих в основе анализируемых сигналов, что позволяет выделять значимые для исследователя ритмы электрической активности мозга, отделяя их от мешающих шумов.
Линейный дискриминантный анализ Фишера
Для объяснения сути линейного дискриминанта необходимо ввести такое понятие, как размерность. В математике это количество независимых параметров, необходимых для идентификации точки пространства. Так, например, топологическая карта абсолютно плоского пространства будет иметь размерность равную 2, т.к. для описания любой точки на ней необходимо задать два независимых параметра – координату по Х и координату по Y.
Стоит заметить, что любой предмет или явление будет обладать рядом измеряемых признаков, которые возможно использовать в качестве координатных осей. Полученное поле или объем будет называться пространством признаков. Таким образом, с точки зрения математики, изучаемый объект будет описываться набором координат, количество которых равно размерности полученного пространства признаков.
Любую размерность можно снизить с любого числа параметров (измерений) до одного, просто проецируя n-мерные данные на прямую. Однако данное действие смешивает отдельные показатели, особенно если они образуют хорошо разделенные компактные группы в изначальном пространстве.
Линейный дискриминант Фишера (Fisher’s linear discriminant, далее – ЛДФ) – математическая операция, предназначенная для снижения размерности пространства признаков с целью упрощения задачи. Его целью является поиск такой ориентации прямой, при которой спроецированные признаки хорошо различимы.
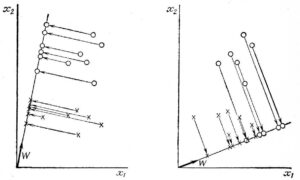
ЛДФ используется с целью получения устойчивого алгоритма классификации при машинном обучении, особенно часто – в случаях недостатка данных. В биомедицинских исследованиях данный метод нашел свое применение в оценке тяжести состояния пациента и прогнозе течения болезни. Для этого в ходе ретроспективного анализа пациенты подразделяются на группы согласно тяжести заболевания. После этого изучаются результаты клинического и лабораторного анализов, чтобы обнаружить переменные, которые достаточно отличаются в изучаемых группах. На основе этих переменных строятся дискриминантные функции, которые помогают объективно классифицировать течение болезни у пациентов в будущем. Для проведения этого анализа возможно применение различного ПО, среди которого стоит выделить такую платформу как RapidMiner – программную платформу для анализа больших данных.
Линейный дискриминантный анализ ЭЭГ
➥ Основаня статья: Линейный дискриминантный анализ
ЛДА (Linear discriminant analysis, LDA) представляет собой обобщение линейного дискриминанта Фишера. Целью данного анализа является распознавание двух классов объектов по некоторому описанию, которое представляется в виде совокупности параметров, на основании которых возможно построение координатного пространства. После создания подобного пространства, координатными осями которого являются параметры исследуемых объектов, оба класса объектов представляются в виде скопления точек в различных областях полученного пространства. Затем для каждого класса производится вычисление “центроида” – воображаемой точки, координаты которой являются средними значениями переменных. Задача дискриминантного анализа в данном случае заключается в построении дополнительной оси координат, которая проходит через облако точек таким образом, что проекции на нее обеспечивают наилучшую разделяемость на два класса. Также необходимо учитывать, что ЛДА работает с независимыми переменными, которые являются непрерывными величинами.
К примеру, на рисунке 27 демонстрируется разделение множества полученных результатов на два подмножества на основании различий в их свойствах. Стоит отметить, что свойства объектов, как указано выше, описывается их положением на координатной плоскости.
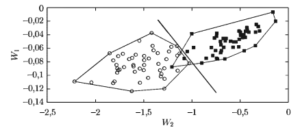
Так же как и ЛДФ, ЛДА нашел свое применение в анализе биологических сигналов. В качестве примера можно привести работу Манило Л.A. и Немирко Л.П. «Сокращение размерности пространства спектральных признаков в многоклассовой задаче распознавания сигналов». В ходе данного исследования рассматривались записи результатов ЭКГ из стандартной компьютерной базы MIT-BIH. В результате анализа на координатной плоскости были отмечены три группы, соответствующие тем или иным диагнозам.
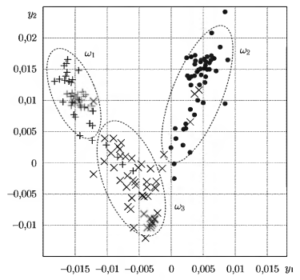
W1— опасные аритмии (желудочковая фибрилляция и трепетание желудочков); w2— пароксизмальная тахикардия и фоновый ритм, представленный разными формами экстрасистолии; w3 — пируэтная тахикардия, являющаяся переходной формой опасного нарушения ритма.
Полученный результат позволил снизить среднюю ошибку классификации данных. В практическом приложении это означает повышение точности интерпретации данных компьютерными программами, использующими данный алгоритм.
Картирование ЭЭГ
➥ Более подробно читайте статью: Картирование головного мозга
Картирование ЭЭГ (EEG mapping) или картирование головного мозга представляет собой создание карт активности нейронов головного мозга с целью выявления патологий или аномалий. В зависимости от способа и цели получения информации, картирование подразделяют на два направления – структурное и функциональное. Задача первого состоит в определении трехмерных пространственных параметров, которые характеризуют анатомическую и биохимическую структуру головного мозга. Второе направление основано на оценке динамических параметров работы мозга – в первую очередь, его электрической активности.
Метод ЭЭГ, равно как и МРТ (магнитно-резонансная томография) и ПЭТ (позитронно-эмиссионная томография), относится к функциональному картированию. Его сущность заключается в регистрации показателей множества пар электродов, которые охватывают всю кору головного мозга. Подобные пары электродов называются отведениями и фиксируются на строго определенных позициях на определенном участке мозга. На основании полученных данных выстраивается совокупность двумерных изображений характеристик ЭЭГ, анализ которых позволяет определить участки аномальной активности в коре головного мозга. Это достигается за счет регистрации изменений нормальных показателей в соответствующих отведениях. Более того, на основе полученных данных возможно выстраивание полноценной топографической карты активности головного мозга.
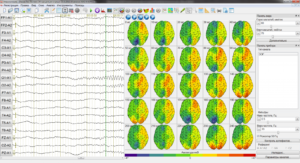
В левой части рисунка 29 представлены данные ЭЭГ в виде графиков зависимости частоты от времени. В центральной части схематически изображен головной мозг и проявляемая его участками активность. Окраска зон зависит от амплитуды сигнала. Применение данного метода в клинической практике позволяет определить зоны патологической активности, что играет важную роль в лечении таких заболеваний, как эпилепсия.
Картирование ЭЭГ фактически является финальным этапом в обработке полученных данных. Суммируя, можно сказать, что данный метод применяется для визуализации электрической активности мозга и определения ее локализации. Это повышает наглядность и упрощает визуальный анализ результатов. Однако у данного метода имеются и недостатки. К таковым относятся: невозможность распознания артефактов и форм потенциалов, отсутствие общепринятых стандартов и высокие требования к квалификации специалиста.
Для устранения некоторых недостатков применяется метод Z-картирования. В данном случае на схему наносятся не распределения мощностей, а показатели среднего квадратичного отклонения (Z) от среднего значения группы нормы данных конкретного исследуемого. В математической статистике под этим термином понимается показатель рассеивания значений некой величины относительно ее ожидания. При превышении этим показателем значения в 2,5, можно говорить о ненормальности электрической активности в этом отведении и в этом частотном диапазоне1516.
Подводя итоги, стоит заметить, что компьютерное картирование активности мозга не является основным методом диагностики и проводится после формулировки заключения на основании анализа обычной ЭЭГ. При обнаружении во время картирования возможных патологий, не выявленных в обычной ЭЭГ, рекомендуется проверка этих данных на артефактность путем сравнения с первоначальными результатами. Постановка диагноза же возможна только после комплексной оценки всей суммы клинико-электрофизиологических данных.
Проведение картирования ЭЭГ возможно с использованием таких аппаратно-программных комплексов как вышеупомянутый «Неврополиграф» или «Нейро-КМ». Первая система использует собственное ПО, поставляемое в комплекте с устройством и позволяющее проводить полномасштабную обработку и анализ поступающих сигналов. Вторая система использует программный комплекс Brainsys, который позволяет проводить спектральный анализ ЭЭГ на основе дискретного преобразования Фурье с графическим представлением и картированием результатов. Что касается непосредственно программного обеспечения, то здесь стоит упомянуть такие программы как EDFbrowser и NeoRec. Обе представляют собой пакеты ПО, предназначенные для записи и обработки файлов ЭЭГ, и имеют модульную структуру, что позволяет настраивать их функционал в широком диапазоне.
Footnotes
- Nunez P.L., Srinivasan R., Wijesinghe R.S., Westdorp A.F., Tucker, D.M., Silberstein R.B., Cadusch P.J. EEG coherency. I: Statistics, reference electrode, volume conduction, Laplacians, cortical imaging, and interpretation at multiple scales. Electroencephalography and Clinical Neurophysiology 1997; 103: 499—515
- Leocani L, Comi G. EEG coherence in pathological conditions. J Clin Neurophysiol. 1999 Nov;16(6):548-55. doi: 10.1097/00004691-199911000-00006.
- Jelic V, Shigeta M, Julin P, Almkvist O, Winblad B, Wahlund LO. Quantitative electroencephalography power and coherence in Alzheimer’s disease and mild cognitive impairment. Dementia. 1996 Nov-Dec;7(6):314-23. doi: 10.1159/000106897.
- Classen J., Gerloff C., Honda M., Hallet M. Integrative Visuomotor Behavior Is Associated With Interregionally Coherent Oscillations in the Human Brain. J Neurophysiol 1998; 79: 1567—1573.
- Кулаичев А.П, Компьютерная электрофизиология и функциональная диагностика. – 4 изд. – М.: Форум: Инфра-М, 2007. – С. 134-146.
- Р. Поликар. “Введение в вейвлет-преобразование”. – СПб.: АВТЭКС, 2010. Автор перевода – Грибунин В.Г.
- Daubechies I. Orthonormal bases of compactly supported wavelets // Communications on Pure and Applied Mathematics. 1988. Vol. 41. P. 909.
- Tass P.A. et al. Detection of n:m phase locking from noisy data: Application to magnetoencephalography // Phys. Rev. Lett. 1998. Vol. 81. P. 3291. 105
- Подробное объяснение терминов см. в Вентцель Е.С. Теория вероятностей. – 10 изд. – М.: Наука, 1969. – С. 84-130.
- Немирко А.П., Манило Л.А., Калиниченко А.Н. Математический анализ биомедицинских сигналов и данных. – М.: ФИЗМАТЛИТ, 2016.
- Chunmei Wang, Junzhong Zou, Jian Zhang, Min Wang, Rubin Wang Feature extraction and recognition of epileptiform activity in EEG by combining PCA with ApEn. [Электрон.ресурс] // Cogn Neurodyn 4:233–240 – 2010. – URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2918747/pdf/11571_2010_Article_9120.pdf (дата обращения 10.11.2020)
- Метод главных компонент // MachineLearning.ru URL: http://www.machinelearning.ru/wiki/index.php?title=Метод_главных_компонент (дата обращения: 10.11.2020).
- Чиликин А. В. Программное обеспечение компьютерной системы анализа вариабельности ритма сердца методом главных компонент. [Электрон.ресурс] // Автоматика. Автоматизация. Электротехнические комплексы и системы – URL: http://aaecs.org/chilikin-a-v-programmnoe-obespechenie-kompyuternoi-sistemi-analiza-varia-belnosti-ritma-serdca-metodom-glavnih-komponent.html:(дата обращения 10.11.2020)
- Акулов Л. Г., Муха Ю. П. Методы обработки электроэнцефалографических данных. [Электрон.ресурс] // ИЗВЕСТИЯ ВолгГТУ – 66 c. – 2008. – URL: http://www-dev.vstu.ru/files/vstu_periodical/1789/upload/2008-04.pdf#page=66 (дата обращения 10.11.2020)
- Nuwer M.R., Jordan S.E. Ahn S.S. Evaluation of stroke using EEG-frequency analysis and topographic mapping. Neurology, 1987, v. 37, p. 1153—1159.
- Seri S., Cerquiglini A., Cusmai R., Curatolo P. Tuberous sclerosis: relationships between topographic mapping of EEG, VEPs and MRI findings / Neurophysiol, clin., 1991, v. 21, p. 161-172