Болезнь Альцгеймера — дегенеративное заболевание центральной нервной системы, характеризующееся прогрессирующим расстройством памяти в начальной стадии процесса, переходящим в глубокое общее слабоумие в конечной стадии. По-видимому, решающим фактором в возникновении первой стадии процесса является утрата холинергических клеток базальными отделами переднего мозга.
Описание поведения
Симптомы
С возрастом нервные клетки медленно умирают. Но в некоторых, к счастью, редких случаях этот естественный медленный процесс значительно ускоряется и ведет к дегенеративным изменениям. В 1906 г. немецкий доктор А. Альцгеймер опубликовал данные наблюдения 51-летней пациенткой с тяжелой деменцией. Он описал поведенческие симптомы и связал их с обнаруженными у этой пациентки патологическими изменениями в коре и лимбической системе. В настоящее время мы знаем о двух основных нейрональных нарушениях при болезни Альцгеймера: утрате холинергических клеток в базальном отделе переднего мозга и развитии сенильных бляшек в коре, локализованных преимущественно в области височных долей.
Медиаторы
Связь с холинергическими и ГАМК-септально-гиппокампальными кругами
Как мы уже знаем, эпизодическая память связана с холинергическими и ГАМК-эргическими септально-гиппокампальными кругами. Эти круги, по-видимому, ответственны за запуск обработки информации в гиппокампе и связанных с ним структурах. Этот гипотетический запуск проявляется в кратковременных вспышках тета-ритма, генерируемого в гиппокампальных кругах. Нарушение генерации вспышек гиппокампального тета-ритма может быть следствием дисфункции перегородки в результате ее анатомической деструкции или воздействия антагонистов ацетилхолина. С гипотезой о роли запуска тета-активности в кодировании информации согласуется наличие связи между подавлением лимбического тета-ритма и нарушением эпизодической памяти.
Холинергическая гипотеза болезни Альцгеймера
Идея о том, что некоторые симптомы болезни Альцгеймера обусловлены дефицитом нейромедиатора ацетилхолина в мозге, впервые возникла в 1976 г., когда Дэвис и Малонэ опубликовали свою статью в журнале Lancet. Последующие работы подтвердили их находки. Согласно холинергической гипотезе болезни Альцгеймера, некоторые когнитивные отклонения у пациентов с этим заболеванием обусловлены дефицитом холинергической нейротрансмиссии. Эта гипотеза стимулировала серьезные исследования в области экспериментальной фармакологии. Большинство препаратов, одобренных к использованию при болезни Альцгеймера Управлением по контролю над пищевыми продуктами и лекарственными средствами США (Food and Drug Administration, FDA) повышает уровень ацетилхолина путем подавления его распада.
Вспышки тета-волн в здоровом мозге
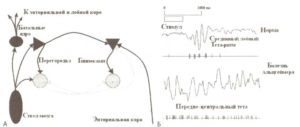
А. Нейронная сеть, вовлеченная в генерацию гиппокампального тета-ритма. Б. Ответы в ЭЭГ (зарегистрированные в Fz) и гипотетическая импульсная активность нейронов в гиппокампе здорового испытуемого (вверху) и у пациента с болезнью Альцгеймера.
На рис. 1 изображены гипотетические нейронные сети, ответственные за консолидацию эпизодической памяти и, возможно, поврежденные при болезни Альцгеймера. Эпизодическая память формируется долговременной потенциацией в гиппокампальных кругах путем повторяющихся вспышек активности гиппокампальных нейронов. Кратковременная активация гиппокампальных нейронов во время привлекающих внимание событий отражается во вспышках тета-ритма в гиппокампе. Эта ритмическая активность передается в переднюю цингулярную кору по мамилло-таламическому тракту и видна в ЭЭГ в форме лобного тета-ритма средней линии. Гиппокампальный тета-ритм управляется септальным входом, так что амплитуда вспышек тета-ритма строго зависит от уровня активации холинергических нейронов в перегородке. Механизм генерации тета-ритма включает тормозные связи между перегородкой и гиппокампом.
Увеличение спонтанной тета-активности в больном мозге
Дегенерация септальных нейронов при болезни Альцгеймера, вероятно, ведет к снижению септального тормозного контроля над гиппокампальными нейронами и, как следствие, к их растормаживанию. Это растормаживание ведет к увеличению спонтанной нейронной активности в гиппокампе (рис. 1). Повышенная гиппокампальная активность, по-видимому, проявляется медленными осцилляциями, обнаруживаемыми в Fz форме колебаний корковых потенциалов в тета-дельта, диапазонах. Эти колебания существенно отличаются от нормального гиппокампального тета-ритма, поскольку они не привязаны по времени к привлекающим внимание стимулам и не имеют отношения к консолидации эпизодической памяти. Более того, утрата тормозного контроля из септального региона может обусловить возникновение эпилептиформной активности в гиппокампе, а в некоторых случаях — эпилептических приступов. В дополнение к этому дегенерация холинергических клеток в базальных ядрах (BN на рис. 1) при болезни Альцгеймера приводит к уменьшению холинергического входа в префронтальную кору из восходящей активирующей системы, что, в свою очередь, может отражаться в повышении медленной активности и уменьшении бета-активности в префронтальных отделах.
Структурные и физиологические корреляты
Количественная ЭЭГ
В работе, выполненной в Университете Тюбенгена А. Стевенсом и его коллегами (Stevens et al., 2001), регистрация 19-канальной ЭЭГ проводилась при закрытых и открытых глазах и при наблюдении за маятником у пациентов с мягкими формами болезни Альцгеймера и у их здоровых сверстников. Значимый эффект различий двух групп по абсолютной мощности и когерентности был выявлен только для тета-диапазона и выражался в увеличении мощности и снижении когерентности у пациентов. Самым надежным параметром для отличия пациентов был параметр когерентности при открытых глазах.
В работе, выполненной недавно в лаборатории Р. Джона в Медицинском колледже Нью-Йоркского университета (Prichep et al., 2005), исследовались данные здоровых пожилых людей с субъективными жалобами на когнитивные расстройства с целью оценки возможности использования ЭЭГ для предсказания клинического ухудшения в течение последующих 7 лет. Спектральные характеристики ЭЭГ у лиц с последующим нарастанием нарушений значимо (р < 0,0001) отличались от таковых улиц со стабильной клинической картиной увеличением абсолютных и относительных значений мощности в тета-диапазоне, замедлением основного ритма и изменениями межрегиональной ковариации.
Когнитивные вызванные потенциалы (ВП)
Компоненты когнитивных ВП также могут использоваться для разграничения пациентов с болезнью Альцгеймера и здоровых лиц. В работе, выполненной в Стэнфордском университете, возрастные и обусловленные деменцией изменения когнитивных ВП оценивались с помощью теста на название картинок (Mathalon et al., 2003). Авторы использовали синхронизированные с ответом ВП в качестве маркеров мониторинга ответа. Старение ассоциировалось с замедлением поведенческих ответов и снижением амплитуды негативности, связанной с ошибкой, в то время как для деменции было характерно уменьшение точности ответов и снижение амплитуды негативности по сравнению со здоровыми ровесниками.
Анализ когнитивных ВП методом главных компонент
В работе, недавно выполненной в Рочестерском университете в США (Chapman et al., 2006), была произведена попытка использования метода главных компонент для анализа когнитивных ВП с целью разграничения пациентов с болезнью Альцгеймера и здоровых лиц. Авторы использовали тест «Число — буква». Помимо известных компонент — РЗЬ, условного негативного отклонения и медленной волны (SW) — авторы сумели выделить другие компоненты, включая относительно ранние пики с латентностью 145 и 250 мс (компонента хранения в краткосрочной памяти). В дискриминантном анализе для создания функции, которая позволила бы успешно разделять индивидов с начальными этапами болезни Альцгеймера и здоровых лиц, использовались параметры когнитивных ВП в ответ на значимые и незначимые стимулы. Применение дискриминантной функции к половине данных показало, что приблизительно 90 % индивидов были корректно отнесены или к группе болезни Альцгеймера или к контрольной группе с чувствительностью 1,00.
Лечение
Ингибиторы ацетилхолинэстеразы
Основная идея современной фармакотерапии болезни Альцгеймера состоит в повышении уровня ацетилхолина в мозге, что обычно достигается путем подавления холинэстераз. Препараты, известные как ингибиторы ацетилхолинэстеразы (ИАХЭ), были одобрены Управлением по контролю над пищевыми продуктами и лекарственными средствами США в 1995 г. после того, как клинические испытания показали умеренное симптоматическое улучшение когнитивных, поведенческих и общих показателей в результате их применения.
ЭЭГ-биоуправнение
Поиск в PubMed с использованием комбинации ключевых слов «Болезнь Альцгеймера» и «ЭЭГ-биоуправление» не обнаружил ни одной статьи касательно использования ЭЭГ-БОС для коррекции симптомов болезни Альцгеймера.
Заключение
Болезнь Альцгеймера — это дегенеративное заболевание мозга, сопровождающееся прогрессирующим снижением памяти. Утрата холинергических клеток в базальном отделе переднего мозга, по-видимому, ответственна за первый этап развития заболевания. Согласно холинергической гипотезе болезни Альцгеймера, некоторые когнитивные отклонения у пациентов с этим заболеванием обусловлены дефицитом холинергической нейротрансмиссии. Большинство препаратов, одобренных к использованию при болезни Альцгеймера Управлением по контролю над пищевыми продуктами и лекарственными средствами США (Food and Drug Administration, FDA), повышают уровень ацетилхолина путем подавления его распада. Дегенерация септальных нейронов при болезни Альцгеймера, по-видимому, ведет к снижению тормозного контроля над гиппокампальными нейронами и, как следствие, к повышению фоновой активности в гиппокампе. Спонтанная гиппокампальная активность проявляется в лобных отведениях в виде тета-колебаний, отличающихся от лобного тета-ритма средней линии. ЭЭГ пациентов с болезнью Альцгеймера характеризуется увеличением абсолютных и относительных значений мощности в тета-диапазоне.